讲授新课
课堂小结
板书
| 一.理想气体
假设有这样一种气体,它在任何温度和任何压强下都能严格地遵从气体实验定律,我们把这样的气体叫做“理想气体”。
思考:理想气体具有那些特点呢?
1、理想气体是不存在的,是一种理想模型。
2、在温度不太低,压强不太大时实际气体都可看成是理想气体。
3、从微观上说:分子间以及分子和器壁间,除碰撞外无其他作用力,分子本身没有体积,即它所占据的空间认为都是可以被压缩的空间。
4、从能量上说:理想气体的微观本质是忽略了分子力,没有分子势能,理想气体的内能只有分子动能。
一定质量的理想气体的内能仅由温度决定 ,与气体的体积无关.
【问题3】如果某种气体的三个状态参量(p、V、T)都发生了变化,它们之间又遵从什么规律呢?
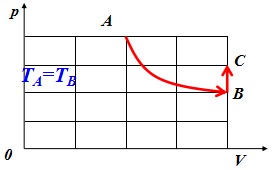
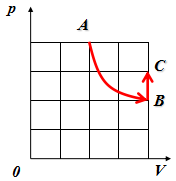
如图所示,一定质量的某种理想气体
从A到B经历了一个等温过程,
从B到C经历了一个等容过程。
分别用pA、VA、TA和pB、VB、TB以及pC、VC、TC表示气体在A、B、C三个状态的状态参量,
那么A、C状态的状态参量间有何关系呢?
推导过程
从A→B为等温变化:由玻意耳定律
pAVA=pBVB
从B→C为等容变化:由查理定律<Object: word/embeddings/oleObject3.bin>
又TA=TB VB=VC 解得:<Object: word/embeddings/oleObject4.bin>
二、理想气体的状态方程
1、内容:一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
2、公式:<Object: word/embeddings/oleObject5.bin>
3、使用条件:一定质量的某种理想气体.
4、气体密度式:<Object: word/embeddings/oleObject6.bin>
说明:<Object: word/embeddings/oleObject7.bin>
方程具有普遍性
①当温度T保持不变<Object: word/embeddings/oleObject8.bin>
②当体积V保持不变<Object: word/embeddings/oleObject9.bin>
③当压强P保持不变<Object: word/embeddings/oleObject10.bin>
课堂练习1、某种气体的压强为2x105 Pa,体积为1 m3,温度为200K。它经过等温过程后体积变为2m3。随后,又经过等容过程,温度变为300 K,求此时气体的压强。
解:根据玻意耳定律,有<Object: word/embeddings/oleObject11.bin>
根据查理定律,有<Object: word/embeddings/oleObject12.bin>
联立上述各式可得<Object: word/embeddings/oleObject13.bin>
<Object: word/embeddings/oleObject14.bin> 等温和等容变化后气体的压强为1.5x105Pa。
三、用状态方程解题思路:
☆明确研究对象——一定质量的气体
☆选定两个状态——已知状态、待求状态
☆列出状态参量:
☆列方程求解
课堂练习2、一水银气压计中混进了空气,因而在27℃,外界大气压为758mmHg时,这个水银气压计的读数为738mmHg,此时管中水银面距管顶80mm,当温度降至-3℃时,这个气压计的读数为743mmHg,求此时的实际大气压值为多少毫米汞柱?
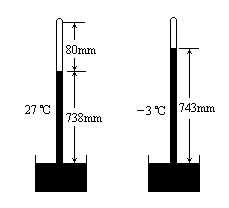
解:以混进水银气压计的空气为研究对象
初状态:p1=758-738=20mmHg V1=80Smm3 T1=273+27=300 K
末状态:p2=p-743mmHg V2=(738+80)S-743S=75Smm3
T2=273+(-3)=270K
由理想气体状态方程得:<Object: word/embeddings/oleObject15.bin>,
<Object: word/embeddings/oleObject16.bin>
解得: p=762.2 mmHg
拓展提高1、气焊用的氧气储存于容积是100 L的筒内,这时筒上压强计显示的压强是60 p0( p0=1.0×105 Pa ),筒的温度是16 ℃,求筒里氧气的质量。已知在温度为0 ℃,压强为p0时,氧气的密度 ρ0=1.43 kg/m3 。
分析:本题的研究对象是筒内一定质量的氧气。由于不知氧气在温度为16 ℃、压强为60 p0下的密度,但知道氧气在温度为0 ℃、压强为p0时的密度,所以要用气体状态方程算出在温度为0 ℃,压强为p0下的体积,再根据密度公式算出氧气的质量。
解析:由理想气体状态方程<Object: word/embeddings/oleObject17.bin>得
<Object: word/embeddings/oleObject18.bin><Object: word/embeddings/oleObject19.bin>
<Object: word/embeddings/oleObject20.bin>
拓展提高2、如果病人在静脉输液时,不慎将5mL的空气柱输入体内,会造成空气栓塞,致使病人死亡.设空气柱在输入体内前的压强为760mmHg,温度为27℃,人的血压为120/80mmHg,试估算空气柱到达心脏处时,在收缩压和扩张压两种状态下,空气柱的体积分别为多少?
解析:空气柱的初状态参量:
p0=760mmHg,V0=5mL,T0=300K.
它在体内收缩压时的状态参量:
p1=120mmHg,T1=310K.
由理想气体状态方程:<Object: word/embeddings/oleObject21.bin>,
一、理想气体:
在任何温度和任何压强下都能严格地遵从气体实验定律的气体
二、理想气体的状态方程
<Object: word/embeddings/oleObject23.bin>
气体密度式:<Object: word/embeddings/oleObject24.bin>
一、理想气体
二、理想气体的状态方程<Object: word/embeddings/oleObject25.bin>
三、用状态方程解题思路:
| 完成思考题,并与同学交流讨论,明确什么是理想气体,特点是什么。
结合前几课学习的气体定律,思考气体在状态A、B、C的状态参量之前的关系。
整体推导过程。
熟悉理想气体状态方程的各种形式。
完成课堂练习
梳理解题思路和方法。
完成课堂练习
完成拓展提高练习题。
梳理本节课知识。
梳理知识结构。
| 通过学生讨论,让学生深刻理解理想气体这一“理想化模型”。
让学生自主研讨,提高学生的交流合作能力,同时也促进学生对新旧知识的掌握和对比。
推导新知识,帮助学生整理思路,加深知识印象。
展示理想气体状态方程的各种形式,加强对状态方程的理解。
强化解题思路,完善解题步骤。
总结知识技能的应用和方法,提高学生解题效率。
强化解题思路,完善解题步骤。
巩固本节课所学的基础知识,并让学生能够灵活应用本节课内容解决实际问题。
课堂小结由学生完成,能帮助学生形成知识框架,更好的理解和应用知识。
展示本节课知识框架,帮助学生记忆。
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图