教学过程
|
教学环节
| 教师活动
| 学生活动
| 设计意图
|
导入新课
|


思考:用什么方法可以使凹进去的兵乓球恢复原状?
打足气的车胎在烈日下暴晒,常常会爆胎,为什么?
车胎内的气体因温度T升高而压强P增大,体积V膨胀。
知识回顾:气体的状态参量
T = t + 273 K
2、体积:体积 V 单位:有L、mL等
3、压强:压强 p 单位:Pa(帕斯卡)
| 车胎内的气体因温度T升高而压强P增大,体积V膨胀。
回顾旧知识:气体,温度,体积,压强
| 用生活现象引入课题,激发学习兴趣,增加学生对本节课内容的亲近感,激发探究欲望,体验物理学科与生活紧密联系。
|
讲授新课
| 思考:一定质量的气体,它的温度、体积和压强三个量之间变化是相互对应的.我们如何确定三个量之间的关系呢?
在物理学中,当需要研究三个物理量之间的关系时,往往采用“保持一个量不变,研究其它两个量之间的关系,然后综合起来得出所要研究的几个量之间的关系”. 。
一、探究气体等温变化的规律
1.等温变化:气体在温度不变的状态下,发生的变化.
2.在等温变化中,气体的压强与体积可能存在着什么关系?(定性关系:观看演示实验)
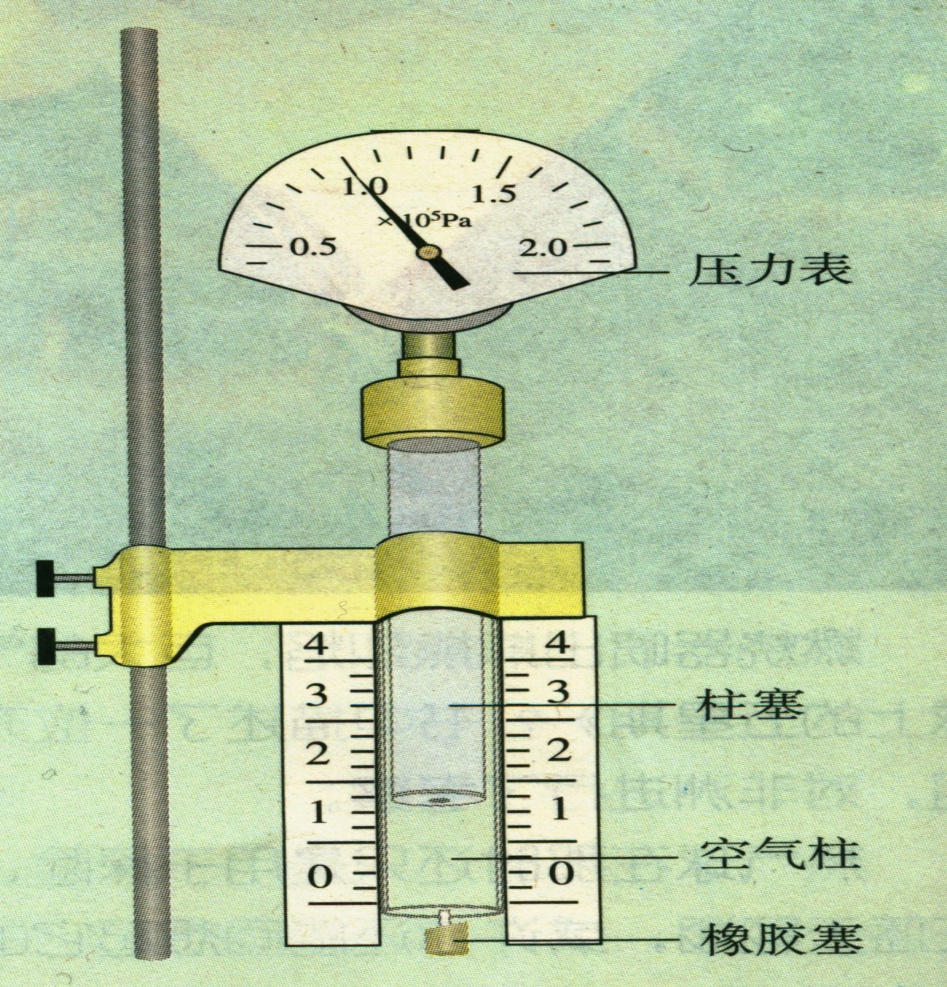
(一)提出问题、引导猜想
结论:V减小,p增大
(二)分组实验、验证猜想
1.实验装置介绍:注射器、气压传感器、平板电脑、数据线。
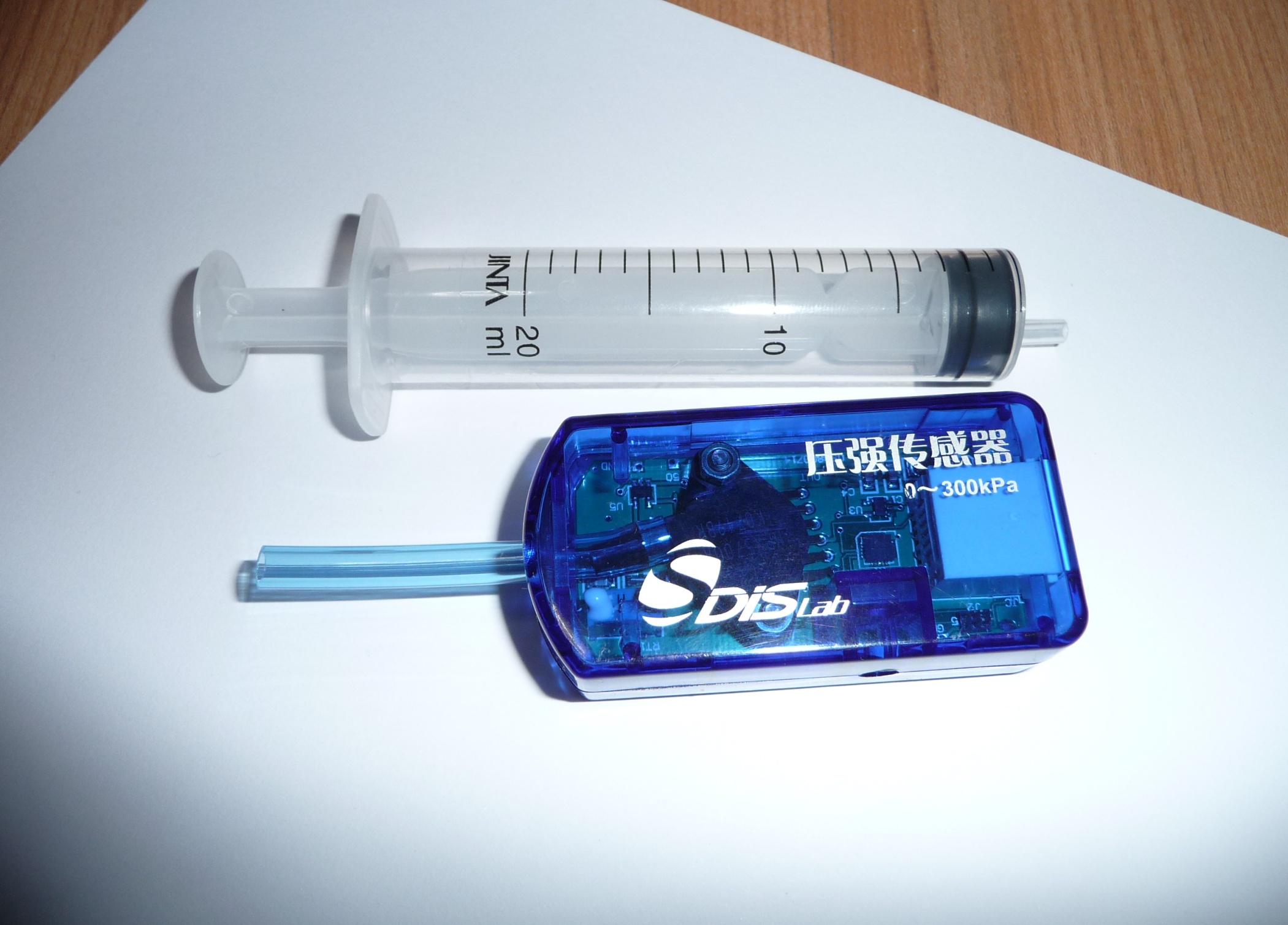
2.注射器的使用注意事项:
(1)连接传感器之前,抽入20mL的气体;
(2)实验时不要用手去摸气体部分;
(3)推拉要缓慢;
(4)读数时眼睛要平视,用左边这条黑线读数。

3.实验仪器使用说明:
(1)将电脑、压强传感器、注射器进行连接;
(2)打开“WCY专用软件”中的 “气体压强与体积的关系”。
(3)点击“开始记录”,抽入20mL的气体,压到10点击点采数据,拉回15点击点采数据,然后20、25、30、35、40分别点采数据
(4)点击 “p-V绘图”,点击“曲线拟合”。
(三)实验数据的处理
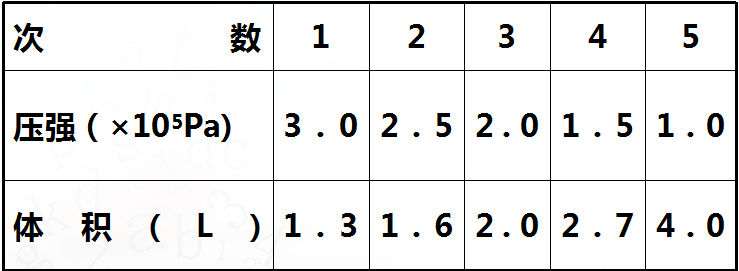
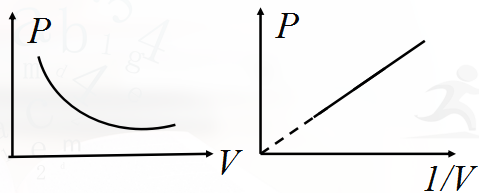
p-V图象
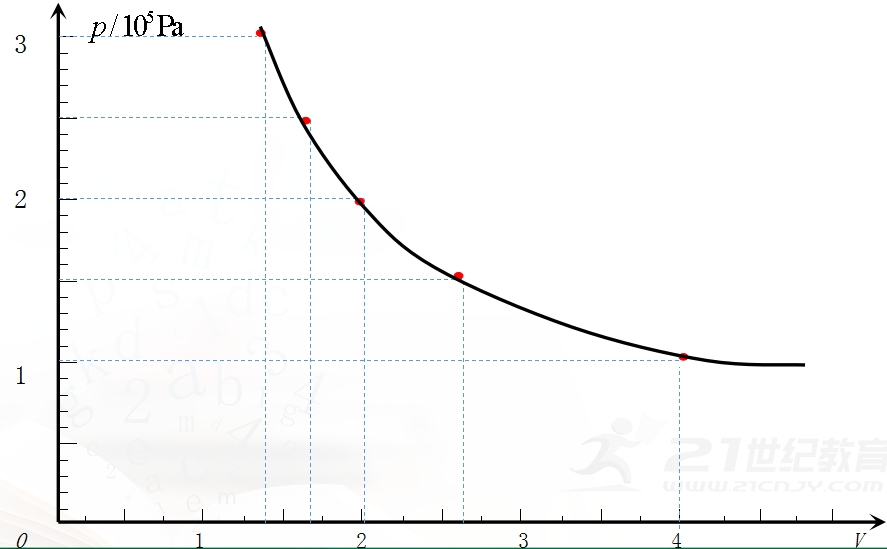
思考:该图象是否可以说明p与V成反比?
如何确定p与V的关系呢?
p-1/V图象
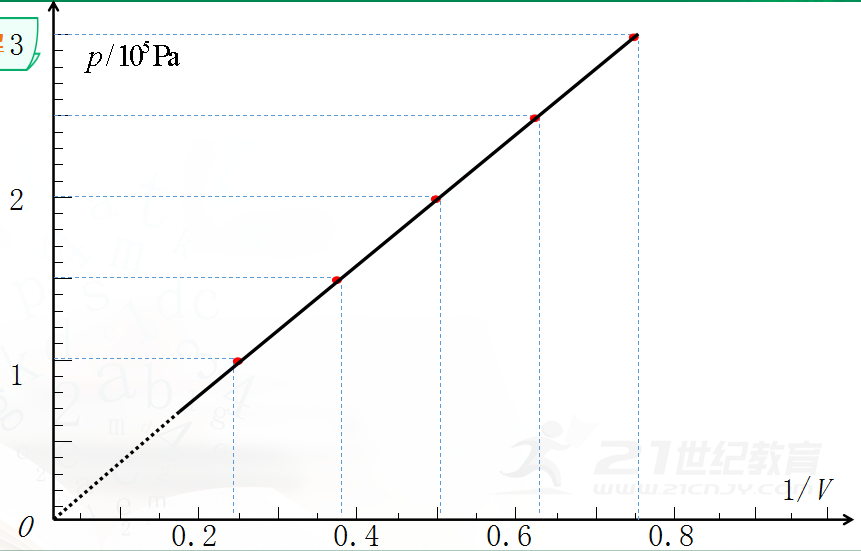
(四)得出结论
结论:在温度不变时,压强p和体积V成反比。
二、玻意耳定律
1、文字表述:一定质量某种气体,在温度不变的情况下,压强p与体积V成反比.
2、公式表述:pV=C(常数 ) 或p1V1=p2V2
3、适用范围:温度不太低,压强不太大
三、气体等温变化的P-V图像
1.等温线:一定质量的理想气体的P-V图像的形状为双曲线的一支,
它描述的是温度不变时的p V关系,称为等温线。
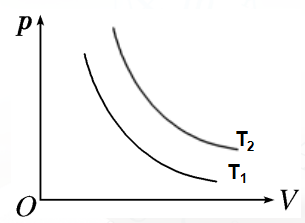
特点:
(1)每条等温线上气体各状态温度相同;
(2)温度越高等温线离坐标轴或原点越远.
思考1:有两条等温线,你能判断哪条等温线表示的是温度比较高时的情形吗?是根据什么理由做出判断的?
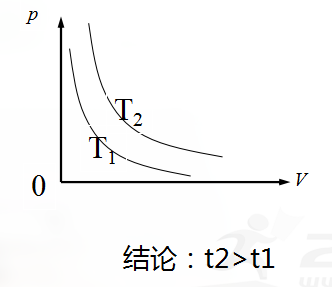
思考2:t1和t2哪个表示的温度高?
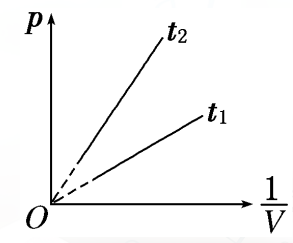
特点:斜率越大温度越高。
课堂练习1、一定质量气体的体积是20L时,压强为1×105Pa。当气体的体积减小到16L时,压强为多大?设气体的温度保持不变。
解析: p1V1=p2V2
答案:1.25×10 5Pa
课堂练习2、如图,一上端开口,下端封闭的细长玻璃管,下部有长l1=66 cm 的水银柱,中间封有长l2=6.6 cm的空气柱,上部有长l3=44 cm的水银柱,此时水银面恰好与管口平齐.已知大气压强为p0=76 cmHg.如果使玻璃管绕底端在竖直平面内缓慢地转动一周,求在开口向下和转回到原来位置时管中空气柱的长度.封入的气体可视为理想气体,在转动过程中没有发生漏气.
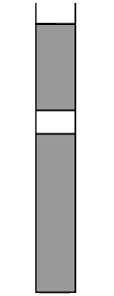
解析:玻璃管开口向上时:p1=p0+ρgl3
玻璃管开口向下时:则p2=ρgl1,p0=p2+ρgx
从开始转动一周后,则p3=p0+ρgx
由玻意耳定律有p1l2S=p2hS p1l2S=p3h′S
解得: h=12 cm h′=9.2 cm
四、用气体定律解题的步骤
1.确定研究对象.被封闭的气体(满足质量不变的条件);
2.用一定的数字或表达式写出气体状态的初始条件(p1,V1,T1,p2,V2,T2);
3.根据气体状态变化过程的特点,列出相应的气体公式(本节课中就是玻意耳定律公式);
4.将各初始条件代入气体公式中,求解未知量;
5.对结果的物理意义进行讨论.
拓展提高1、如图所示,是一定质量的某种气体状态变化的p-V图象,气体由状态A变化到状态B的过程中,气体分子平均速率的变化情况是( )
A.一直保持不变
B.一直增大
C.先减小后增大
D.先增大后减小
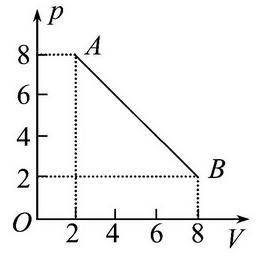
解析:分子平均速率由温度决定,在图中画出等温线可知:pV先增大后减小,则T先增大后减小,
答案:C
拓展提高2、某个容器的容积是10L,所装气体的压强是20×105Pa。如果温度保持不变,把容器的开关打开以后,容器里剩下的气体是原来的百分之几?设大气压是1.0×105Pa.
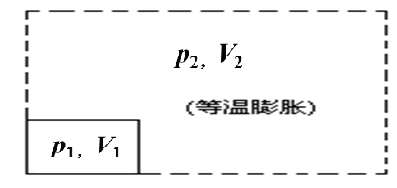
解析:初态 p1=20×105Pa V1=10L T1=T
末态 p2=1.0×105Pa V2=?L T2=T
由玻意耳定律 p1V1=p2V2得 V2=200L
剩下的气体为原来的5%
点评:就容器而言,里面气体质量变了,似乎是变质量问题了,但若视容器中气体出而不走,就又是质量不变了.
3.如图所示为一定质量的气体在不同温度下的两条P-1/V图线.由图可知( )
A.一定质量的气体在发生等温变化时,其压强与体积成正比
B.一定质量的气体在发生等温变化时,其 图线的延长线是经过坐标原点的
C.T1>T2
D.T1<T2
解析:温度越高,其等温线离原点越远.
答案:BD
| 控制变量的方法
体验后得出定性关系:一定质量的气体,在温度不变的情况下,体积减小,压强增大;体积增大,压强减小。
猜想: p、V成反比
学生利用电脑三人为一组,进行合作实验。
学生利用电脑处理实验所得的数据。
得出:
p-V关系图象,形状似双曲线的一支。
学生得出:
p-1/V关系图象是一条几乎通过原点的直线。
完成思考题。
完成课堂练习。
完成课堂练习。
整理解题步骤,明确解题思路。
完成本节课拓展提高。
| 通过亲身体验,深刻体会气体压强与体积定性关系,进而激发对定量关系的探究欲望。
练习使用先进仪器进行实验探究规律,体会科学探究过程,培养学生相互协作的精神。
培养学生交流的意愿和能力。通过对实验数据的分析与评估,培养学生严谨的科学态度与实事求是的精神。
培养学生化曲为直的方法和知识迁移的能力。
让学生意识到玻意耳定律使用的局限性。
通过等温线更好的理解玻意耳定律的内容。
锻炼解决实际问题的能力。
整理解题步骤,明确解题思路。
巩固本节课所学知识
|
课堂小结
| 一、玻意耳定律
1、内容:一定质量某种气体,在温度不变的情况下,压强P与体积V 成反比。
2、公式: PV=C(常数) 或p1V1=p2V2
3、条件: 一定质量气体且温度不变
4、适用范围:温度不太低,压强不太大
二、等温变化图象
1、特点:
(1)等温线是双曲线的一支
(2)温度越高,其等温线离原点越远
2、图象意义:
(1)物理意义:反映压强随体积的变化关系
(2)图像上每点的意义: 每一组数据---反映某一状态
| 学生总结本节课学习的内容。
| 课堂小结由学生完成,能帮助学生形成知识框架,更好的理解和应用知识。
|
板书
| 一、玻意耳定律
公式: PV=C(常数) 或p1V1=p2V2
条件: 一定质量气体且温度不变
二、等温变化图象
1、特点:
(1)等温线是双曲线的一支
(2)温度越高,其等温线离原点越远
2、图象意义:
每一组数据---反映某一状态
| 梳理知识结构。
| 展示本节课知识框架,帮助学生记忆。
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图