教学过程(表格描述)
|
教学环节
| 主要教学活动
| 设置意图
|
一、
引入
| 通过改变物质的浓度可以时浓度商发生改变,改变温度,可以使K发生变化,都能使QK,从而使平衡发生移动,那么,改变压强,化学平衡会怎样移动呢?
| 回忆旧知,使学生进一步利用K、Qc大小关系来分析平衡移动。
|
二、
探究压强改变对平衡移动的影响
| 一定条件下,对于任意可逆反应:
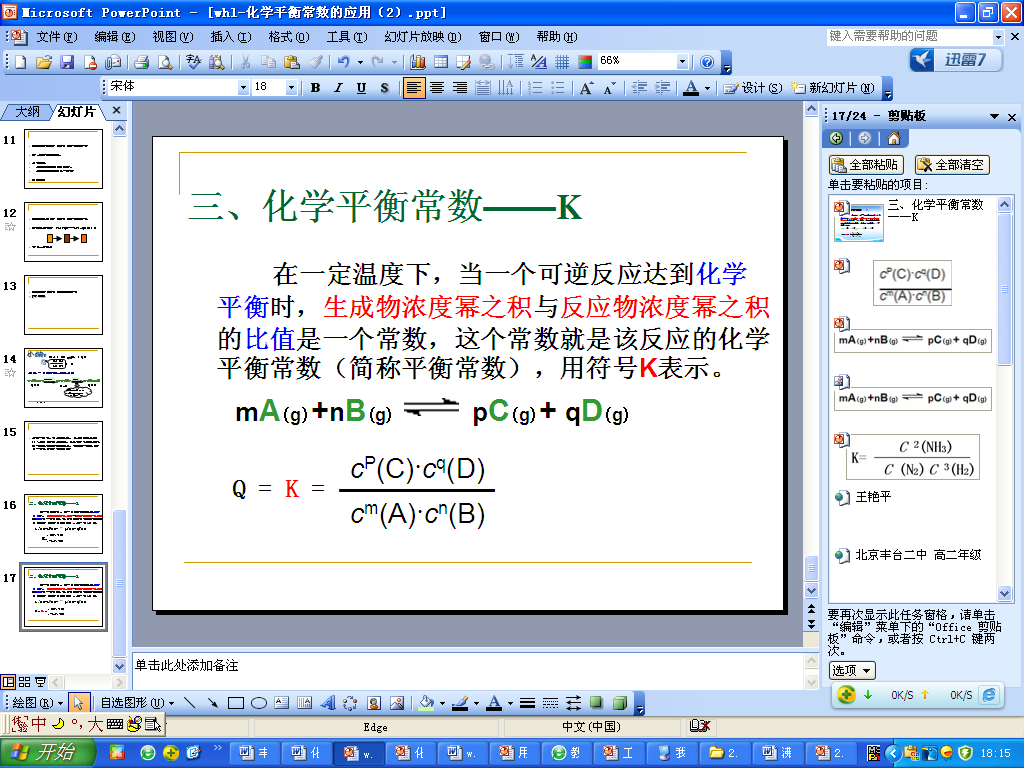
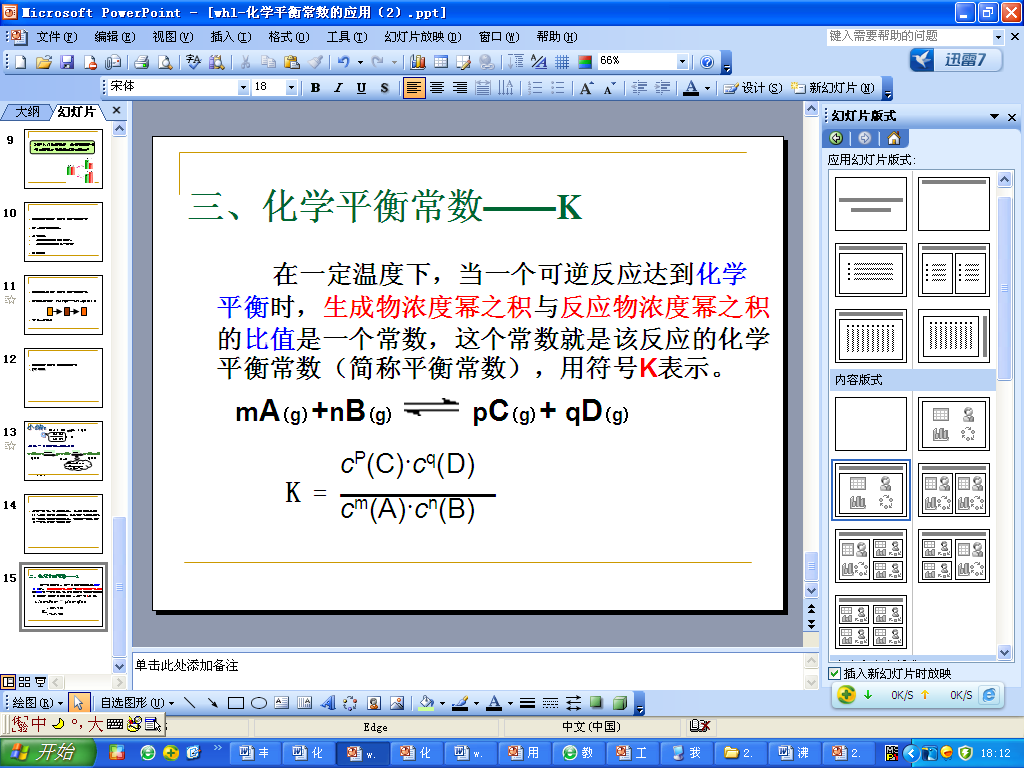 K=
K=
【思考】压强的改变,本质上是改变了浓度商还是改变了平衡常数呢?
平衡常数只受温度影响,温度不变,平衡常数不变。
而压强的改变,是通过压缩容器体积或者增大容器体积来实现的,本质上是同等程度的改变了各物质的浓度,这样看来,各物质的浓度发生改变后,浓度商如何变化呢?
| 引导学生理解压强改变的实质是各物质的浓度改变,进而分析浓度商的变化趋势,并且与平衡常数对比后,演绎推理、归纳总结出平衡移动的方向。
|
| 【理论预测】用Qc-K工具分析下列反应,当体系压强加倍(体积减半)时,将会使平衡怎样移动?
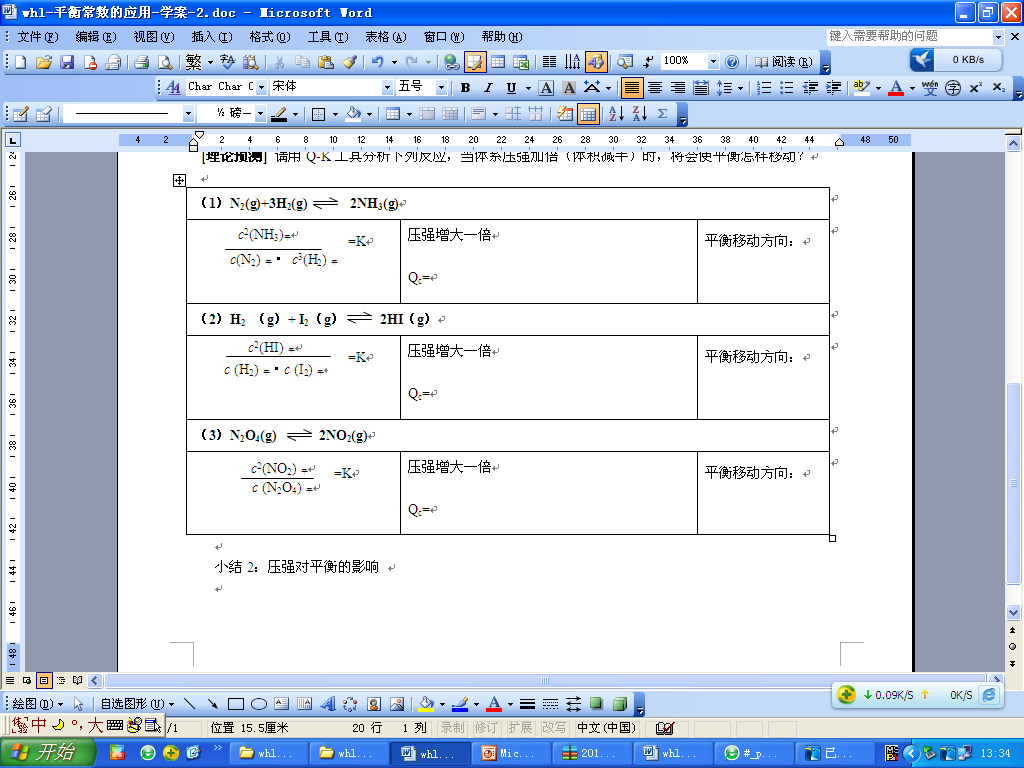
小结:压强对平衡的影响。
| 应用Qc-K关系,分析压强对平衡的影响,再一次体会浓度商的计算方法,并比较Qc-与K的关系,判断出改变压强,平衡的移动方向。
|
三、
勒夏特勒原理
| 勒夏特勒原理的内容;
勒夏特列原理是经过反复验证过的一条科学规律,在化学工业和环境保护技术中都有着十分重要的实际应用。
| 归纳总结,提炼平衡移动原理的精华,感受
|
课堂小结
| 通过今天的学习,如何调控
N2(g)+3H2(g) 2NH3(g), 使氨气产量更高?
还有什么因素可以使平衡正向移动?。
| 感受原理对实际化学生产的指导作用。
|
课堂练习
| 略
| |
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图