课程基本信息
|
课例编号
| 19
| 学科
| 化学
| 年级
| 高二
| 学期
| 第一学期
|
课题
| 弱电解质的电离 盐类水解
|
教科书
| 书名: 化学选择性必修1《化学反应原理》
出版社:山东科学技术出版社 出版日期:2020年 07 月
|
教学目标
|
教学目标:1.通过回顾化学平衡常数,让学生知道电离平衡常数的相关知识,对电离平衡建立定量的认识。2.通过分析温度、浓度、外加物质对电离平衡的影响,学会分析外界条件对弱电解质溶液电离平衡移动分析的一般思路。3.通过“联想·质疑”“观察·思考”“交流·研讨”等活动,体会到综合、分析、归纳等方法在解决水溶液问题中的应用。
教学重点:温度、浓度、外加物质对电离平衡的影响。
教学难点:温度、浓度、外加物质对电离平衡的影响。
|
教学过程
|
时间
| 教学环节
| 主要师生活动
|
| 环节一
联想质疑
提出问题
| 通过“联想·质疑”问题的提出,引出本节两个研究主题“定量表示弱电解质电离能力-电离平衡常数”和“影响电离平衡的因素”。
|
| 环节二
复习旧知
引出新知-电离平衡常数
| 【师】复习回顾化学平衡相关知识,引入表征弱电解质电离的程度的常数-电离平衡常数。
【生】参照化学平衡,以醋酸为例,完成关于电离平衡常数相关内容的表格。
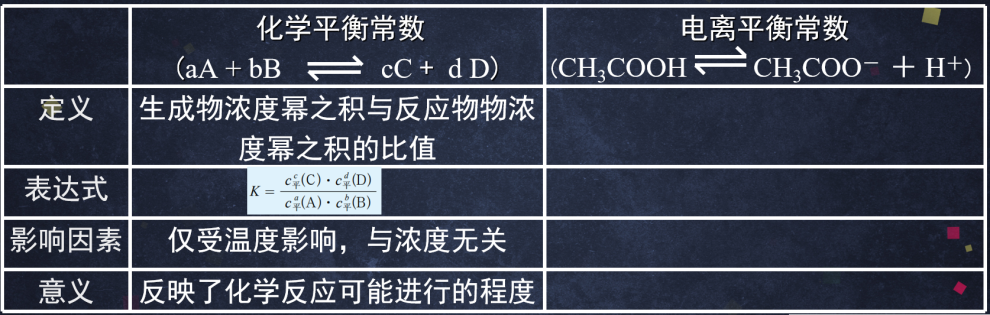
【师】概括整合电离平衡常数定义、表示形式、影响因素及意义。
|
| 环节三
讨论影响的因素
分析平衡移动
| 【师】提出交流研讨问题“哪些因素能影响电离平衡?”
【生】回顾影响化学平衡的外界因素温度、浓度、压强,对于弱电解质稀溶液,不需要考虑压强对电离平衡的影响,指出影响弱电解质电离平衡的外界因素应为温度和浓度。
【师】提出“观察表 3-2-2 给出的数据,可以得出什么结论?”
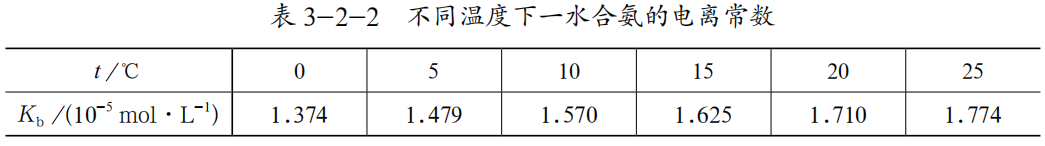
【生】随着温度的升高,一水合氨的电离常数在不断增大,这就意味着一水合氨的电离平衡在正向移动。依据“升高温度使吸热反应的平衡常数 K 增大,平衡向吸热反应方向移动”的相关知识,判断弱电解质电离方向的焓变为正值,电离过程为吸热过程。温度升高,平衡常数增大,电离平衡正向移动。
【师】微热 0.05 mol·L-1CH3COOH 溶液,CH3COOH 的电离平衡如何移动,下面表格中各量会如何变化呢?

【生】填写上表,体会温度对电离平衡以及各组分浓度的影响。
【师】提出“在 1 mol·L-1 CH3COOH 溶液加水稀释的过程中,表格中各量会如何变化呢?”

【生】交流探讨,产生疑问:“在加水稀释的过程中,各组分浓度都在减小,如何对电离平衡的移动方向进行分析呢?”
【师】加水稀释的过程,溶液在变稀,那么离子相互碰撞结合成分子的机会就越小,弱电解质的电离程度就越大。同学们还有没有别的办法,也可以判断出加水稀释弱电解质的电离平衡会向电离方向移动呢?
【生】通过比较平衡常数K与浓度商Q的大小关系得出移动方向。
 【师】现有 0.1 mol·L-1 的 CH3COOH 溶液,判断当下列条件改变时溶液中发生的变化。
【师】现有 0.1 mol·L-1 的 CH3COOH 溶液,判断当下列条件改变时溶液中发生的变化。

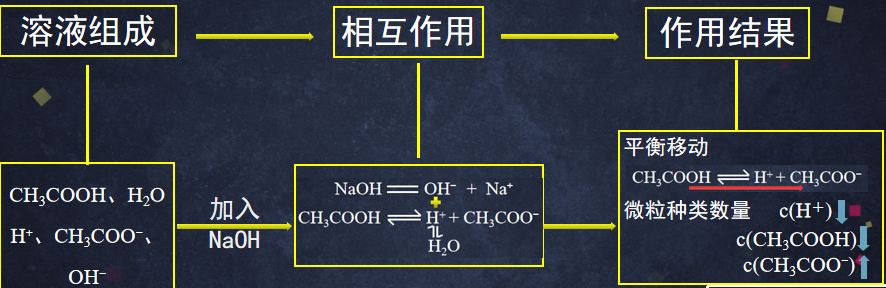
【生】分析外加三种电解质的情况下,平衡的移动方向和离子浓度的变化。
【师】总结分析弱电解质溶液体系的一般思路
【师】常温时,在 pH=2,体积相同的 HCl、CH3COOH 溶液中,分别加入等质量的镁条,若反应停止后,有一份溶液中镁条有剩余,则镁条有剩余的应为盐酸还是醋酸溶液?两支试管中产生氢气的体积谁更多?
【生】通过列方程计算及平衡移动分析,得出最终镁条有剩余的应为装有盐酸的试管,装有醋酸溶液的试管产生的氢气更多。
|
| 环节四
课堂小结
|
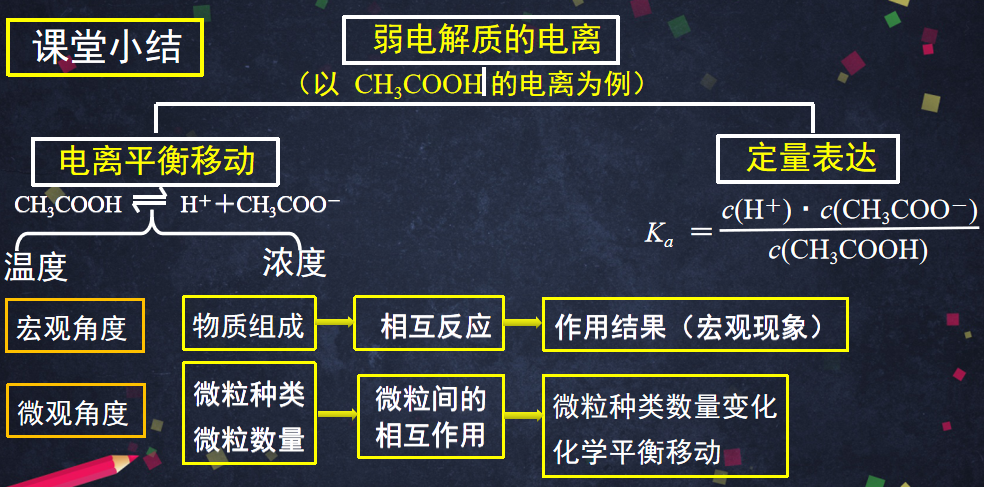
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图