|
|
第一节原子结构与元素性质
第2课时核外电子排布原子结构与元素原子得失电子能力

1.了解原子核外电子的排布,能画出1~20号元素的原子结构示意图。
2.了解原子的核外电子排布与元素的原子得失电子能力和化合价的关系

原子核外电子排布的规律,原子结构与元素原子的失电子能力

1.核电荷数==
2.质量数=+
3.核素的定义。
4.同位素的定义。

一.原子结构
2.核外电子排布
【自学探究】阅读教材P5页内容,归纳总结在含有多个电子的原子里,电子是如何分层排布的?有什么规律?
总结:(1)原子核外电子根据能量由低到高顺序分别在距原子核由到的不同区域运动。
(2)把核外电子运动的不同区域看做不同的,共有电子层,其符号分别为。各电子层上电子的能量不同。电子层离原子核越近其层上电子能量越,越远能量高。
【交流研讨】观察稀有气体元素原子核外电子排布情况,讨论解决以下问题:
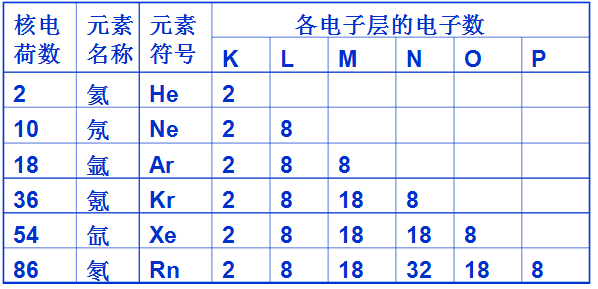
1.核外电子总是先排哪一个电子层。
2.各电子层上最多可容纳电子的数目是多少?和该电子层的序数(用n表示)有何关系?
3.最外电子层、次外电子层及倒数第三电子层最多可容纳的电子数目是多少?
总结:(1)原子核外电子总是先排能力的电子层,然后有里向外,依次排布即排满了层才能排L层,排满了层才能排M层。
(2)原子核外每个电子层最多容纳个电子(n为电子层序数)
(3)原子最外层电子数不超过个电子(K层为最外层时,不超过个电子)。
(4)原子次外层电子数不超过个电子。
(5)倒数第三层不超过个电子
【观察思考】观察1—20号元素原子结构示意图,你能否写出钠离子和氯离子得结构示意图?
【方法导引】离子结构示意图与原子结构示意图写法相同,只是因为原子在形成离子时,会失去最外层电子或最外层得到电子,因此核内质子数不等于核外电子数。
Na+ Cl-
【总结】核外电子排布的表示方法
(1)原子结构示意图核外电子数=
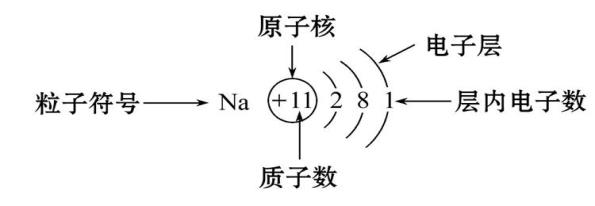
(2)离子结构示意图
阳离子:核外电子数=
阴离子:核外电子数=
【迁移运用】
1. 下列微粒结构示意图表示的各是什么微粒?
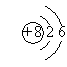
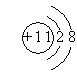
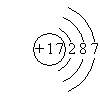
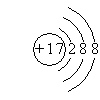
2. 下列微粒结构示意图是否正确?如有错误,指出错误的原因。
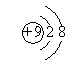
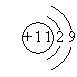
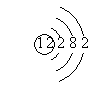
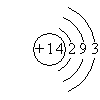
【自学探究二】自学教材第六页前两段内容,小组交流总结元素的性质与原子核外电子排布的关系。
元素性质与原子最外层电子关系
(1)稀有气体元素原子最外层电子数位(He为),不易电子,易显价。
(2)金属元素,最外层电子一般小于,易电子形成阳离子,易显价。
(3)非金属元素,最外层电子一般大于,易得电子形成阴离子,易显价。
【活动探究】
1.预测钠、镁两种元素原子的得失电子能力强弱,并从原子结构的角度说明理由。
2.预测钠、钾两种元素原子的得失电子能力强弱,并从原子结构的角度说明理由。
【实验探究】
【思考】
1.你对以上两组元素原子失电子能力强弱的预测正确吗?你从原子结构的角度对它们失电子能力强弱的解释是否合理?哪些证据支持了你的预测和解释?
2.通过前面的学习,你已经可以从质子数、中子数、核电荷数、核外电子数、最外层电子数、电子层数等方面描述原子的结构了,它们是否会影响元素原子失电子能力的强弱?如果会,如何影响?如果不会,说明理由。
3.请根据以上讨论来分析说明硫、氯两元素中哪种元素原子的得电子能力强。
【迁移应用】
镁和铝在金属活动性顺序表中均排在氢之前,但是二者分别与盐酸反应的速率、现象不一样,①中反应剧烈,②中反应不剧烈。
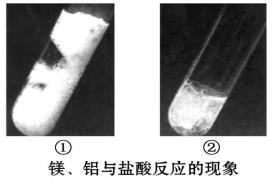
- 根据图示以及镁、铝的电子层结构分析,哪个图表示的是镁与盐酸的反应?
(2)试利用原子结构的观点解释反应剧烈的一方剧烈的原因是什么?

1.下列关于原子核外电子排布规律的说法错误的是 ( )
A.K层是能量最低的电子层
B.原子失电子时先失去能量低的电子
C.核外电子总是优先排布在能量较低的电子层上
D.N层为次外层时,最多可容纳的电子数为18
2.下列说法中肯定错误的是( )
A.某原子K层上只有一个电子
B.某原子M层上电子数为L层上电子数的4倍
C.某离子M层上和L层上电子数均为K层上电子数的4倍
D.某离子的核电荷数与最外电子层上的电子数相等
3.下列叙述中正确的是( )
A.电子的能量越低,运动区域离原子核越远
B.核外电子的分层排布即是核外电子的分层运动
C.稀有气体元素原子的最外层都排有8个电子
D.当M层是最外层时,最多可排布18个电子
4.下列粒子的结构示意图中,错误的是( )
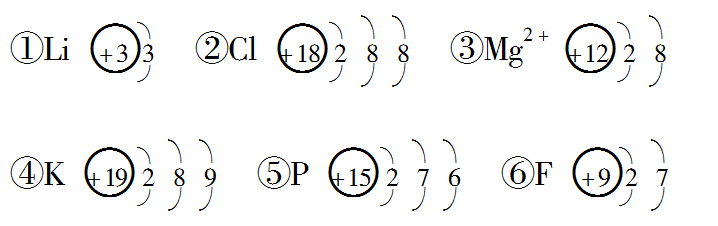
A.②③④⑤ B.①④⑤⑥
C.①②⑤⑥ D.①②④⑤
5.核电荷数为1~20的元素中,下列叙述正确的是 ( )
A.原子最外层只有1个或2个电子的元素一定是金属元素
B.核外电子排布完全相同的两种微粒化学性质一定相同
C.原子核外各层电子数相等的元素不一定是金属元素
D.核电荷数为17的元素容易获得1个电子
6.下列说法不正确的是( )
A.钠和钾最外层电子数相同,故失电子能力相同
B.钠失电子能力比钾弱,是因为钠的电子层数比钾少,原子核对外层电子吸引力比钾强
C.镁原子最外层电子数比钠多,故失电子能力比钠强
D.镁常温下不易和水反应,是因为镁核电荷数比钠的大,对最外层电子吸引力比钠强。
7.写出下列微粒的符号及结构示意图:
①原子核内有10个质子的原子________,
②核外有10个电子的二价阳离子________,
③核外有18个电子的一价阴离子________,
④L为最外层,L层电子数是K层电子数的3倍的原子________。
检测反馈答案
1.【解析】距原子核由近到远,电子的能量由低到高,即离原子核近的电子能量低,离原子核远的电子能量高,则K层是能量最低的电子层,A正确;原子最先失去最外层电子,最外层电子的能量最高,所以原子失电子时先失去能量高的电子,B错误;核外电子总是优先排布在能量较低的电子层上,C正确;电子层的次外层最多容纳18个电子,所以N层为次外层时,最多可容纳的电子数为18,D正确。
【答案】选B。
2.【解析】 K层、L层、M层上最多能容纳的电子数分别为2、8、18。K层上可排1个电子,也可排2个电子,所以A项有可能;当M层上排有电子时,L层已经排满电子,即排了8个电子,而M层最多可以排18个电子,所以B项错误;符合“某离子M层上和L层上电子数均为K层上电子数的4倍”的离子可以是S2-、Cl-、K+、Ca2+等,C项正确;对D项来说,最外电子层上的电子数可为2或8,核电荷数和最外层电子数均为2的只有He,不符合条件,核电荷数和最外层电子数均为8的为O2-,所以D项有可能。
【答案】 B
3.【解析】 在离核较近区域内运动的电子能量较低,A错误;核外电子的分层排布即是核外电子的分层运动,B正确;氦原子最外层只有2个电子,C错误;任何电子层作最外层时,所容纳的电子均不超过8个,D错误。
【答案】 B
4.【解析】 ①错误,K层最多只能容纳2个电子;②错误,Cl的核电荷数为17;④错误,最外层电子不能超过8个;⑤错误,L层上电子为8个,M层上电子为5个。
【答案】 D
5.【解析】在核电荷数为1~18的元素中,最外层只有1个电子的元素有H、Li、Na、K,其中H为非金属元素,最外层只有2个电子的元素有He、Be、Mg、Ca,其中He为稀有气体元素,A项错误;核外电子排布完全相同的微粒S2-和K+化学性质不相同,S2-具有还原性,K+不具有还原性,B项错误;原子核外各层电子数相等的只有Be,它是金属元素,C项错误;核电荷数为17的元素的原子结构示意图为
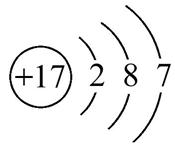 ,其最外层有7个电子,很容易获得1个电子而成为8个电子的稳定结构,D项正确。
,其最外层有7个电子,很容易获得1个电子而成为8个电子的稳定结构,D项正确。
【答案】 D
6.答案:AC
6.答案:
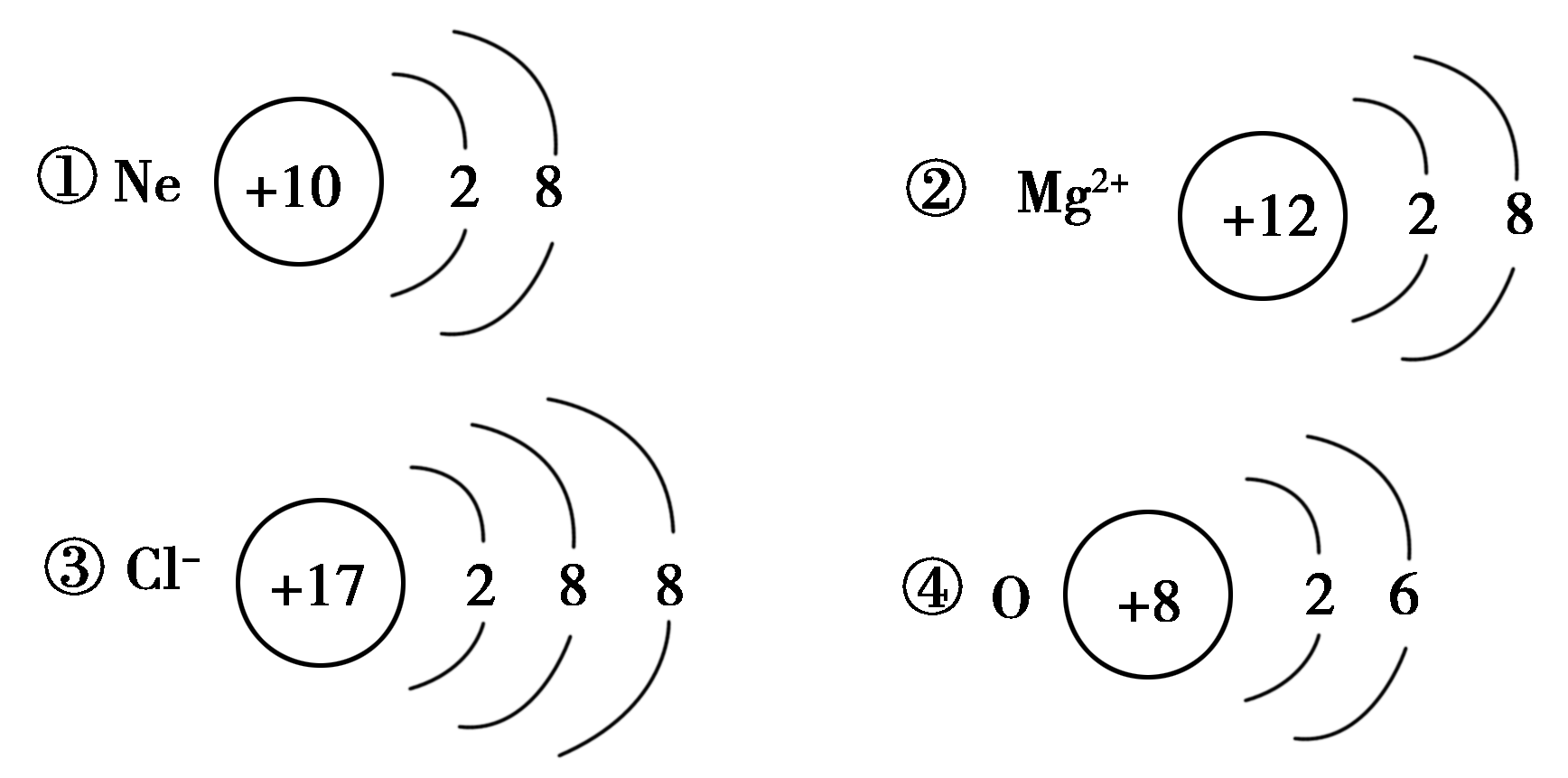
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图