|
|
第三章 简单的有机化合物
第3节 饮食中的有机化合物

1.了解乙酸的物理性质,体会乙酸与日常生活的紧密联系以及研究有机化合物的价值。
2.认识乙酸的分子结构,能正确书写乙酸的结构式、结构简式及其官能团
3.掌握乙酸的化学性质 ,能书写乙酸酸性和酯化反应所对应的化学方程式

乙酸的化学性质及相关的化学方程式

1.乙醇的结构式;结构简式;官能团名称。
2.乙醇的燃烧方程式:。
3.乙醇催化氧化的化学方程式:。
4.乙醇和钠反应的方程式:。

二.乙酸
【自主探究】阅读教材P106页内容,观察所给的乙酸试剂和模型,总结归纳 乙酸的物理性质和结构特点。
1.乙酸的物理性质
乙酸是一种有味的色体,20 ℃时的密度为;沸点为
117.9 ℃,熔点为 16.6 ℃ ;无水乙酸又称 。
2.乙酸的结构
分子式;结构式;结构简式;官能团。
【活动探究】探究乙酸的性质
以小组为单位,结合课本P107页“活动探究”要求,探究乙酸的化学性质
3.乙酸的化学性质
【实验探究一】乙酸的酸性乙酸在溶于水时能够电离出 CH3COO - 和 H+ ,因而乙酸具有一定的酸性。请小组内合作利用所给的试剂设计几个实验证明乙酸具有酸性。完成下面表格(可不填满)
总结:
(1)乙酸的酸性
①;
②;
③;
④;
⑤;
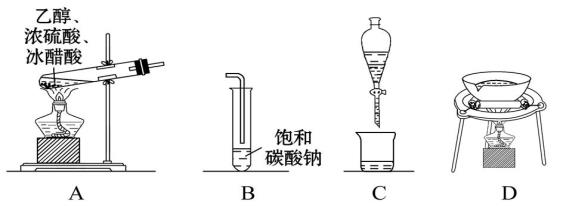
【实验探究二】在试管中加入无水乙醇、浓硫酸、冰醋酸的混合物,再加入2~3块碎瓷片。按图3-3-6
所示连接装置,用酒精灯小心均匀地加热试管,将产生的气体经导管通到饱和Na 2 CO 3 溶液的
液面上。观察发生的现象,闻一闻生成物的气味。
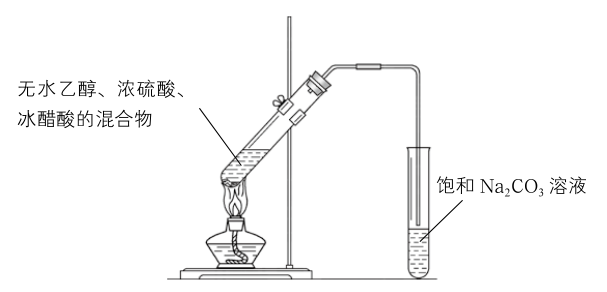
现象: 。
结论: 。
反应方程式: 。
酯化反应:。
酯化反应原理:酸脱去,醇脱去。
【交流研讨】
a.反应中浓硫酸的作用是什么?碎瓷片的作用是什么? 。
b.为什么反应物都必须是无水液体? 。
c.为什么要用饱和 Na2 CO 3 溶液吸收产物? 。
d.为什么导气管不能伸入饱和 Na 2 CO3 溶液中? 。
【迁移应用】
1. 向结有水垢[主要成分是 CaCO3 和 Mg(OH)2 ]的壶里或暖瓶里加入少量食醋(最好是醋酸),浸泡一段时间后,再用水清洗,水垢便可除去。请写出相关反应的化学方程式。
2. 用粮食酿制的酒中,除了含有乙醇,通常还含有少量乙酸等物质。由粮食酿造的酒会随着储藏时间的延长而变得更醇香,请分析其中可能的原因。

1.下列说法正确的是( )
A.乙酸的官能团是羟基
B.可用紫色石蕊溶液鉴别乙醇和乙酸
C.可用食醋除去水壶中的水垢(以CaCO3为主)
D.制取乙酸乙酯时,适当增大乙醇的浓度,可使乙酸完全反应
2.下列不属于乙酸用途的是 ( )
A.杀菌消毒 B.生产香料
C.调味剂 D.检验司机是否是“酒后驾车”
3.下图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。该物质不具有的性质是 ( )
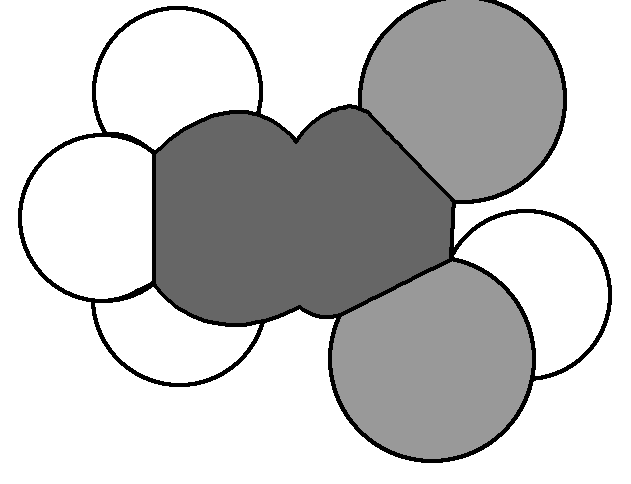
A.与氢氧化钠反应 B.与稀硫酸反应
C.发生酯化反应 D.使紫色石蕊溶液变红
4.下列说法正确的是 ( )
A.酯化反应也属于加成反应
B.酯化反应中羧酸脱去羧基中的羟基,醇脱去羟基中的氢原子生成水
C.浓硫酸在酯化反应中只起催化剂的作用
D.欲使酯化反应生成的酯分离并提纯,可以将酯蒸气通过导管伸入饱和碳酸钠溶液的液面下,再用分液漏斗分离
5.以下用于除去乙酸乙酯中乙酸和乙醇杂质的最好试剂是 ( )
A.饱和碳酸钠溶液 B.氢氧化钠溶液
C.苯 D.水
6.如图为实验室制取少量乙酸乙酯的装置图,下列关于该实验的叙述中,不正确的是 ( )
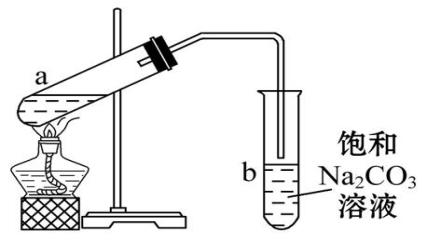
A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
B.试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
C.实验时加热试管a的目的是及时将乙酸乙酯蒸出并加大反应速率
D.采用长玻璃导管有导气兼冷凝的作用
7.某有机物的结构如图所示,这种有机物可能具有的性质是 ( )
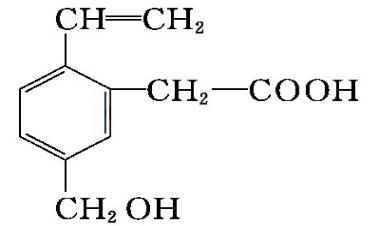
①可以燃烧 ②能使酸性KMnO4溶液褪色 ③能跟NaOH溶液反应 ④能发生酯化反应 ⑤能发生加成反应 ⑥能发生取代反应
A.①②③④⑤ B.①③④⑥ C.①②⑤ D.全部
8.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是 ( )
9.等物质的量的下列有机物与足量金属钠反应,消耗金属钠的质量从大到小的顺序是________。等物质的量的下列有机物与足量的NaHCO3浓溶液反应,产生的气体的体积从大到小的顺序是________。
①CH3CH(OH)COOH
②HOOC—COOH
③CH3CH2COOH
④HOOC—CH2—CH2—CH2—COOH
10.实验室合成乙酸乙酯的步骤如下:
在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得一含有乙醇、乙酸和水的乙酸乙酯粗产品。
请完成下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入________,目的是________。
(2)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
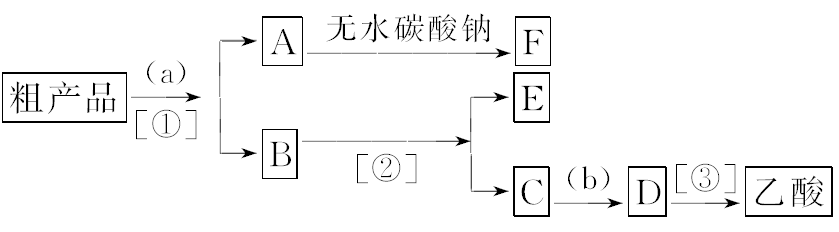
试剂a是________,试剂b是________;分离方法①是______。分离方法②是________,分离方法③是________。
(3)在得到的A中加入无水碳酸钠粉末,振荡,目的是________。
检测反馈答案
1.【答案】BC
2.【答案】D
【解析】检验司机是否是酒后驾车的装置中含有橙色的酸性重铬酸钾,当其遇到乙醇时由橙色变为蓝绿色。
3.【答案】B
【解析】由比例模型知,该物质为CH3COOH,显酸性,能使紫色石蕊溶液变红,能与NaOH反应,能与醇发生酯化反应,故选B项。
4.【答案】B
5.【答案】A
【解析】饱和碳酸钠溶液能溶解乙醇,吸收乙酸,同时降低乙酸乙酯的溶解度。
6. 【答案】A
【解析】A项中,浓硫酸和其他液体混合时,应将浓硫酸慢慢加到密度比它小的溶液中,应先向a中加入乙醇和冰醋酸,然后边摇动试管边慢慢加入浓硫酸。B项中,加热过程中产生乙酸和乙醇蒸气,二者溶于Na2CO3溶液易造成倒吸。C项,加热一方面能加大反应速率,另一方面能及时将乙酸乙酯蒸出,有利于提高反应物的转化率。D项,长玻璃导管既能导出乙酸乙酯蒸气,又能冷凝回流挥发出的乙酸和乙醇。
7. 【答案】D
【解析】该有机物含碳碳双键,可使酸性KMnO4溶液褪色,能发生加成反应;含—COOH,可发生酯化反应,能与NaOH溶液反应;大多数有机物都可以燃烧;含—COOH、—OH,二者均可发生酯化反应,而酯化反应也属于取代反应。
8. 【答案】D
【解析】乙酸乙酯的制备实验中由于最终得到的乙酸乙酯不能溶解在水中,所以分离的方法是分液而非蒸发,所以答案选D。
9.【答案】①=②=④>③ ②=④>③=①
【解析】有机物分子里的羟基和羧基都可以和Na反应放出H2,则消耗金属钠的质量①=②=④>③;而只有羧基和NaHCO3溶液反应放出CO2,所以产生的气体的体积②=④>③=①。
10.【答案】(1)碎瓷片 防止暴沸 (2)饱和Na2CO3溶液 稀硫酸 萃取、分液 蒸馏 蒸馏 (3)除去乙酸乙酯中的水分
【解析】只要熟悉乙酸乙酯制取实验,就比较容易答好第一个小题。对于第(2)和(3)小题,可从分析粗产品的成分入手。粗产品有乙酸乙酯、乙酸、乙醇三种物质,用饱和碳酸钠溶液进行萃取、分液可把混合物分离成两种半成品,其中一份是乙酸乙酯(即A)、另一份是乙酸钠和乙醇的水溶液(即B)。蒸馏B可得到乙醇(即E),留下残液是乙酸钠溶液(即C)。再在C中加稀硫酸,经蒸馏可得到乙酸溶液。
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图