讲授新课
| 第三节 分子结构与物质的性质
第三课时 氢键、溶解性、手性分子
一、氢键及其对物质性质的影响
1.定义:它是由已经与电负性很大的原子(如N、F、O)形成共价键的 氢原子与另一分子中电负性很大的原子之间的作用力。
2.表示: 氢键通常用X—H…Y —表示,“—”表示共价键,“…”表示形成的氢键(X、Y为N、O、F)如

3.形成条件:分子中一定要有N、O、F这三种原子中的一种,或者含有N—H键、O—H键、F—H键中的一种。
注意:一般来说,能形成氢键的元素有N、O、F。所以氢键一般存在于含N—H、H—O、H—F的物质中,或有机化合物中的醇类和羧酸类等物质中。
4.形成原理:
当H原子与N、O、F这三种原子中的一种原子形成共价键时,由于N、O、F的电负性很大,将共用电子对强烈地吸引过来,而使H原子带有较高的正电性(δ+)。此时,H原子与另一分子中的N、O、F(δ—)便存在了一种静电作用。这就是氢键。
5.氢键的特征
氢键不属于化学键,是一种特殊的分子间作用力。氢键键能较小,约为共价键的十分之几,但比范德华力 强;氢键具有一定的饱和 性和方向性。
(1)饱和性:由于H原子半径比A,B的原子半径小得多,当H与一个B原子形成氢键A—H···B 后,H周围的空间被占据,A,B的电子云排斥作用将阻碍另一个B原子与H靠近成键,即H只能与一个B形成氢键,氢键具有饱和性。
H 的体积小,1 个 H 只能形成1个氢键
(2)方向性:A—H与B形成分子间氢键时,3个原子总是尽可能沿直线分布,使A,B尽量远离,这样电子云排斥作用最小,体系能量最低,氢键最强,最稳定,所以氢键具有方向。
6. 氢键强弱
X—H----Y强弱与X和Y的电负性有关:电负性越大,则氢键越强。
如F原子电负性最大,因而F-H----F是最强的氢键; 原子吸引电子能力不同,所以氢键强弱变化顺序为:
F—H----F > O—H----O > O—H----N > N—H----N
注意:C原子吸引电子能力较弱,一般不形成氢键。
7. 氢键的分类
(1)分子间氢键
氢键普遍存在于已经与N、O、F形成共价键的氢原子与另外的N、O、F原子之间。
如:HF、H2O、NH3 相互之间
C2H5OH、CH3COOH、H2O相互之间
(2)分子内氢键
某些物质在分子内也可形成氢键,例如当苯酚在邻位上有—CHO、—COOH、—OH和—NO2时,可形成分子内的氢键,组成“螯合环”的特殊结构。
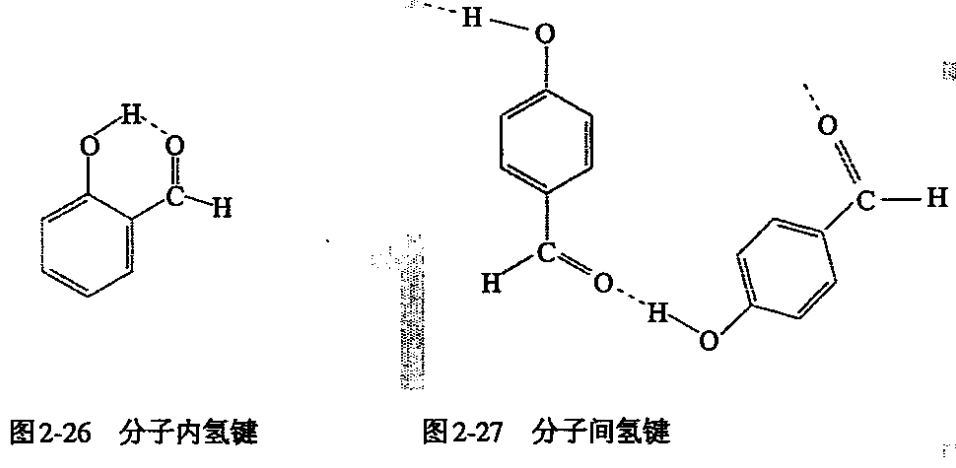
邻羟基苯甲醛在分子内形成了氢键,在分子间不存在氢键。而对羟基苯甲醛不可能形成分子内氢键,只能形成分子间氢键。因而,前者的沸点低于后者的沸点。
8.键长: A—H···B ,指A B之间的距离。
9.键能: A—H···B 分解为A—H和B所需要的能量。
10.本质:分子间作用力!比范德华力的力量要大,比化学键的力量要小,因此氢键只能影响物理性质(如熔沸点高低)。
11. 氢键对物质性质的影响
①氢键主要影响物质的熔、沸点,某些氢化物分子间可以形成氢键,如H2O、NH3、HF等,氢键会使这些氢化物沸点较高,如H2O>H2Te>H2Se>H2S。
②分子间氢键使物质熔、沸点升高,分子内氢键使物质熔、沸点降低。
③氢键对物质溶解性的影响
a.影响物质溶解性的外界因素主要有温度、压强等。
b.相似相溶规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。如蔗糖和氨易溶于水,难溶于四氯化碳;萘和碘易溶于四氯化碳,难溶于水。
c.氢键:溶剂和溶质之间的氢键作用力越大,溶解性越好(填“越好”或“越差”)。
d.分子结构的相似性:溶质和溶剂的分子结构相似程度越大,其溶解性越好。如乙醇与水互溶,而戊醇在水中的溶解度相对较小。
12.水中的氢键对水的性质的影响
(1)水分子间形成氢键,增大了水分子间的作用力,使水的熔、沸点比同主族元素中H2S的熔、沸点高。
(2)氢键与水分子的性质
①水结冰时,体积增大,密度减小。
②接近沸点时形成的“缔合”分子水蒸气的相对分子质量比用化学式H2O计算出来的相对分子质量大。
范德华力与氢键的对比
范德华力
氢键
- 分子间氢键与分子内氢键两种,二者效果相反,前者升高,后者降低
表2-9 某些氢键的键能和键长
氢键X-H…Y
| 键能(kJ/mol)
| 键长(pm)
| 代表性例子
| F-H…F
| 28.1
| 255
| (HF)n
| O-H…O
| 18.8
| 276
| 冰
| O-H…O
| 25.9
| 266
| 甲醇、乙醇
| N-H…F
| 20.9
| 268
| NH4F
| N-H…O
| 20.9
| 286
| CH3CONH2
| N-H…N
| 5.4
| 338
| NH3
|
尽管人们把氢键也称作为键,但与化学键比较,氢键属于一种较弱的作用力,比化学键的键能小1-2个数量级,不属于化学键。
二、分子间作用力对物质性质的影响——溶解性
(1)分子间作用力对物质熔、沸点的影响。
一般来说,组成和结构相似的分子构成的物质,相对分子质量越大,分子间作用力越大,物质的熔、沸点越高。
(2)分子间作用力对物质溶解性的影响。
①“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。如蔗糖和氨易溶于水,难溶于CCl4,因为蔗糖、氨、水都是极性分子;而萘和碘易溶于CCl4,难溶于水,因为萘、碘和CCl4都是非极性分子。离子化合物是强极性物质,很多易溶于水。
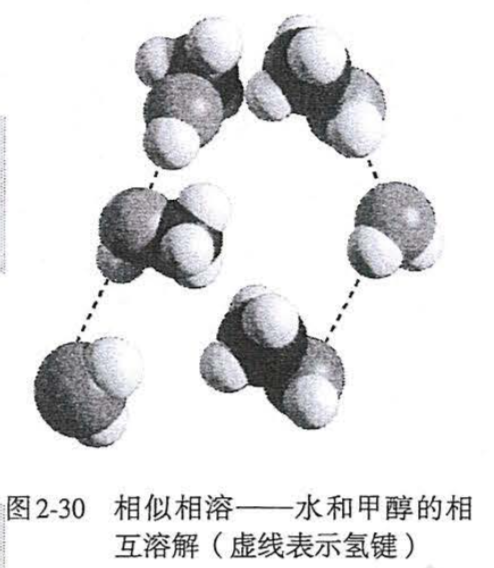
②氢键:若溶剂与溶质分子之间可以形成氢键,则溶解性好;若溶质分子不能与水分子形成氢键,在水中溶解度就相对较小。如NH3极易溶于水,甲醇、乙醇、甘油、乙酸等能与水混溶,就是因为这些物质的分子与水分子之间能够形成氢键。
③分子结构的相似性:“相似相溶”还适用于分子结构的相似性。如乙醇分子中的—OH与水分子中的—OH相近,因而乙醇能与水互溶。当然,乙醇分子由于—OH的极性较强,能与H2O形成氢键也是其互溶的原因。而戊醇(CH3CH2CH2CH2CH2OH)分子中的烃基较大,烃基是非极性基团,是疏水亲油基团,导致戊醇在水中的溶解度比乙醇小。烃基越大的醇在水中的溶解度就越小,羧酸也是如此。
④反应:如果溶质与水能发生化学反应,也会增大溶质的溶解度。如SO2与水发生反应生成H2SO3,而H2SO3可溶于水,因此,SO2的溶解度较大。
【思考与讨论】
(1)比较NH3与CH4在水中的溶解度,怎样用相似相溶规律理解它们的溶解度不同?
极性大的易溶于极性大的溶剂。没有极性的或弱极性的易溶于没有极性的溶剂中。水是极性溶剂, CH4是没有极性的分子, NH3是极性分子,所以NH3易溶于水, CH4不溶于水。
(2)为什么在日常生活中用有机溶剂(如乙酸乙酯等)溶解油漆而不用水?
油漆是非极性分子,有机溶剂如乙酸乙酯也是非极性溶剂,而水为极性溶剂,根据“相似相溶”规则,应当用有机溶剂溶解油漆而不能用水溶解油漆。
(3)在一个小试管里放入一小粒碘晶体,加入约5ml蒸馏水,观察碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约1ml四氯化碳,振荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。再向试管里加入1ml浓碘化钾水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里可发生如下反应:I2+I-=I3-。实验表明碘在纯水还是在四氯化碳中溶解性较好?为什么?
实验表明碘在四氯化碳溶液中的溶解性较好。这是因为碘和四氯化碳都是非极性分子,非极性溶质一般能溶于非极性溶剂,而水是极性分子。
三、分子的手性
观察一下两组图片,有何特征?
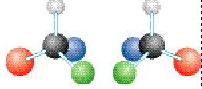
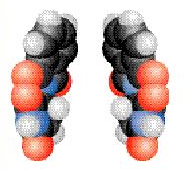
特点:
①具有完全相同的组成和原子排列
②互为镜像,在三维空间里不能重叠
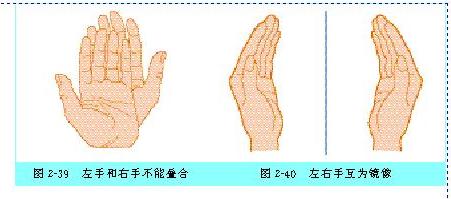
1.手性异构体:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,却在三维空间里不能重叠,互称手性异构体(或对映异构体)
2.手性分子:有手性异构体的分子叫做手性分子。
手性分子在生命科学和药物生产方面有广泛的应用。对于手性药物,一个异构体可能是有效的,而另一个异构体可能是无效甚至是有害的。
手性分子的判断方法
(1)观察实物分子与其镜像能否重合,如果不能重合,说明是手性分子,两种分子互称手性异构体(或对映异构体)。如图:
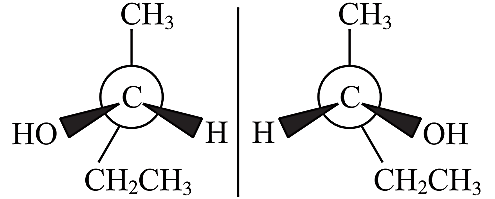
(2)观察有机物分子中是否有手性碳原子,如果有一个手性碳原子,则该有机物分子就是手性分子,具有手性异构体。含有两个手性碳原子的有机物分子不一定是手性分子。
具有手性的有机物,是因为含有手性碳原子造成的。
如果一个碳原子所联结的四个原子或原子团各不相同,那么该碳原子称为手性碳原子,记作﹡C 。
注意:也有一些手性物质没有手性碳原子
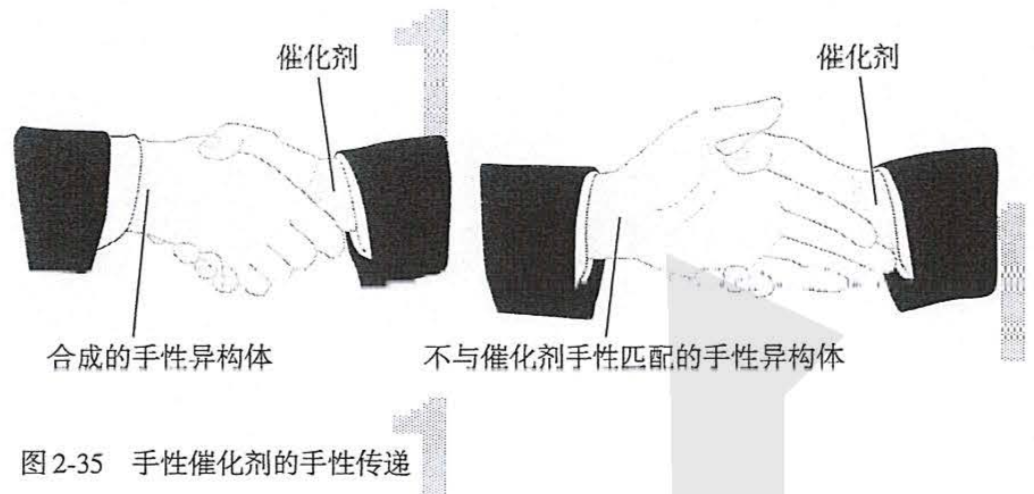
【资料】2001年,诺贝尔化学奖授予三位用手性催化剂生产手性药物的化学家。用他们的合成方法,可以只得到或者主要得到一种手性分子,这种独特的合成方法称为手性合成。手性催化剂只催化或者主要催化一种手性分子的合成,可以比喻成握手——手性催化剂像迎宾的主人伸出右手,被催化合成的手性分子像客人,总是伸出右手去握手。
【课堂练习】
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
①氢键的形成都会使物质的熔、沸点升高。 ( )
②氢键是一种特殊的化学键,它广泛存在于自然界中的物质中。( )
③HF的沸点较高,是因为H—F键的键能很大。( )
④CH4难溶于水,NH3易溶于水。( )
⑤HOCH2CH2OH比CH3OH在水中的溶解度小。( )
⑥分子
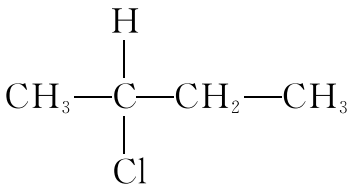 中含有两个手性碳原子。答案: (1)× (2)× (3)× (4)√ (5) × (6) ×
中含有两个手性碳原子。答案: (1)× (2)× (3)× (4)√ (5) × (6) ×
2.物质在不同溶剂中的溶解性,一般遵循“相似相溶”规律。下列装置中,不宜用作HCl尾气吸收的是( )
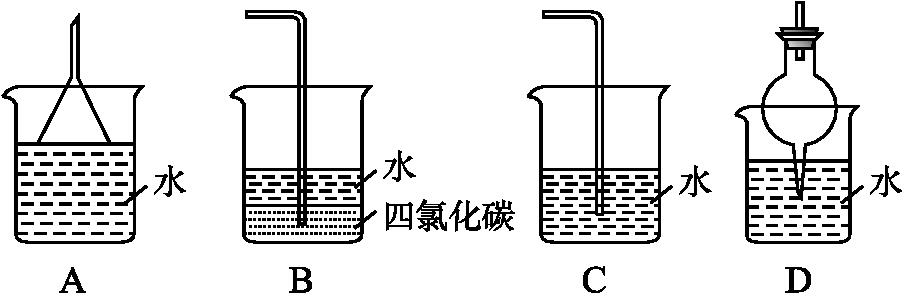
答案:C。A、D项装置可防止倒吸;B项因HCl不溶于CCl4,也可防止倒吸;利用C项装置吸收HCl会发生倒吸,容易引发实验事故。
3.下列关于氢键的说法正确的是( )
A.由于氢键的作用,使NH3、H2O、HF的沸点高于同主族其他元素气态氢化物的沸点
B.氢键只能存在于分子间,不能存在于分子内
C.根据氢键键能的大小可知,沸点高低顺序为HF>H2O>NH3
D.相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多
答案:A NH3、H2O、HF在与其同族简单氢化物中,沸点相对较高,其原因是NH3、H2O、HF分子之间可以形成氢键,A项正确;氢键可以存在于分子间,也可以存在于分子内,B项错误;沸点高低还与分子间可以形成的氢键数目有关,根据通常情况下三种物质的存在状态,可知三种物质中水的沸点最高,C项错误;气态物质分子间距离大,分子之间不能形成氢键,D项错误。
4.下列物质不存在手性异构体的是( )
A.BrCH2CHOHCH2OH
<Object: word/embeddings/oleObject1.bin>C.CH3CHOHCOOH
D.CH3COCH2CH3
答案:D 解析:若同一个碳原子上连接四个不同的原子或原子团,则该碳原子称为手性碳原子,含有一个手性碳原子的物质存在手性异构体。D项中物质不含手性碳原子,不存在手性异构体。
5.下列说法错误的是( )
A.卤化氢中,以HF沸点最高,是由于HF分子间可以形成氢键
B.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低
C.H2O的沸点比HF的沸点高,是由于水分子间形成的氢键键能大
D.氨气极易溶于水与氨气分子和水分子之间可以形成氢键有关
答案:C。 因HF分子间可以形成氢键,所以沸点:HF>HI>HBr>HCl,A正确;邻羟基苯甲醛可以形成分子内氢键,而对羟基苯甲醛的氢键只存在于分子间,所以对羟基苯甲醛的熔、沸点高,B正确;根据F原子半径小于O原子半径,可知(HF)n中氢键键长比水中氢键键长小、键能大,但由于一个HF分子只能与两个相邻的HF分子形成氢键,而一个H2O分子可与四个相邻的H2O分子形成氢键,故H2O的沸点比HF的沸点高,C错误;氨气在水中的溶解性与NH3分子和H2O分子之间形成氢键有关,D正确。
6.下列物质的分子中不具有手性碳原子的是( )
<Object: word/embeddings/oleObject2.bin>B.氨基乙酸:H2N—CH2—COOH
C.丙醛糖:CH2OH—CH(OH)—CHO
D.α-氨基丙酸:CH3—CH(NH2)—COOH
答案:B 解析:有机分子中连接四个不同原子或原子团的碳原子称为手性碳原子。A、C、D选项的分子中,处于中间位置的碳原子均连有一个氢原子和三个不同的其他原子团,该碳原子是手性碳原子,不符合题意;B项分子中间的碳原子上连有两个氢原子,不是手性碳原子。
|
认真思考
思考
认真思考
思考讨论
| 通过对氢键概念的学习,理解氢键的形成以及表示方法,掌握氢键对物质物理性质的影响。
了解氢键的特征。
归纳总结
理解分子内氢键与分子间氢键的形成原理。
通过具体例子理解分子间作用力对物质物理性质的影响。
通过日常经验,结合所学知识,理解物质溶解性的差异原因。
应用
类比理解手性的概念。
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图