讲授新课
| 第二节 分子的空间结构
第三课时 杂化轨道理论简介
一、杂化轨道理论
当碳原子与4个氢原子形成甲烷分子时,碳原子的2s轨道和3个2p轨道会发生混杂,混杂时保持轨道总数不变,却得到4个新的能量相同、方向不同的轨道,各指向正四面体的4个顶角,夹角109°28',称为sp3杂化轨道,表示这4个轨道是由1个s轨道和3个p轨道杂化形成的。
当碳原子跟4个氢原子结合时,碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C-H σ键,因此呈正四面体形的空间结构。
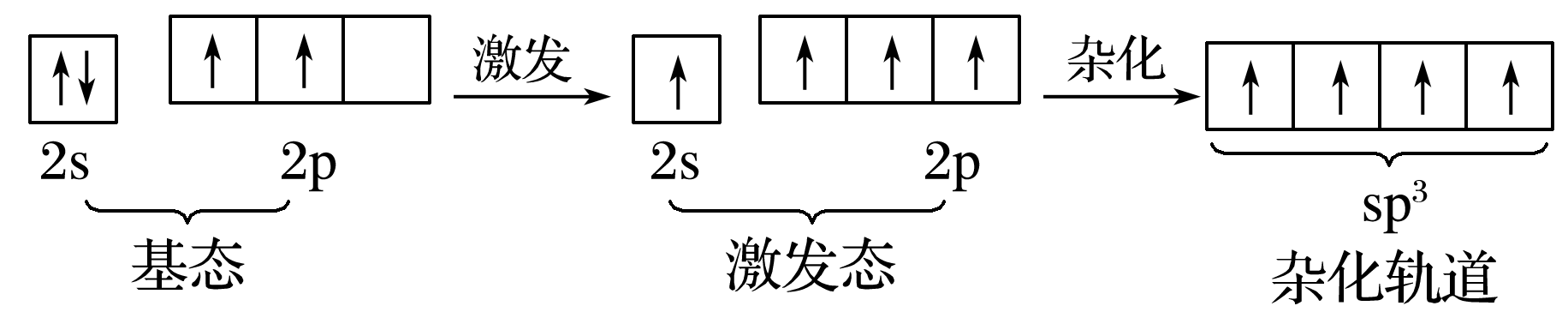
杂化轨道理论是一种价键理论,是鲍林为了解释分子的空间结构提出的。
1.概念:轨道的杂化是指在外界条件影响下,原子内部能量相近的原子轨道发生混杂,重新组合成一组新的轨道的过程。
杂化轨道:原子轨道杂化后形成的一组新的原子轨道,叫做杂化原子轨道,简称杂化轨道。
2.轨道杂化的过程:激发→杂化→轨道重叠。
3.要点:
- 原子在成键时,同一原子中能量相近的原子轨道可重新组合成杂化轨道。
- 杂化改变了原子轨道的形状、方向。杂化使原子的成键能力增加。
- 杂化前后原子轨道数目不变(参加杂化的轨道数目等于形成的杂化轨道数目),且杂化轨道的能量相同。
e) 原子轨道的杂化只有在形成分子的过程中才会发生,孤立的原子不可能发生杂化。
f) 杂化轨道用于形成σ键或者用来容纳未参与成键的孤电子对。未参与杂化的p轨道可用于形成π键。分子的空间结构主要取决于原子轨道的杂化类型。
g) 杂化轨道数=中心原子上的孤电子对数+与中心原子结合的原子数。
4.杂化轨道的形成及其特点

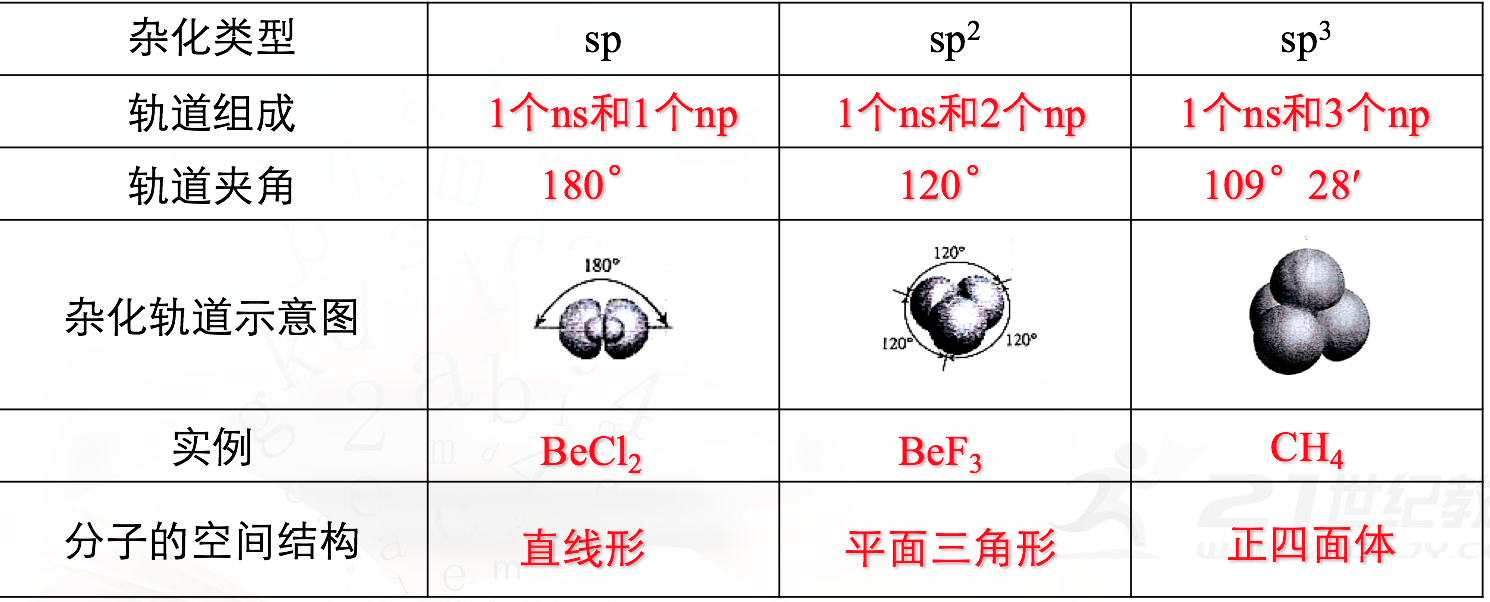
5.杂化轨道的类型
(1) sp3杂化轨道——CH4分子的形成
sp3杂化轨道是由一个ns轨道和三个np轨道杂化而得。sp3杂化轨道的夹角为109°28′,呈空间正四面体形(如CH4、CF4、CCl4)。
(2) sp2杂化轨道——BF3分子的形成
①sp2杂化轨道是由一个ns轨道和两个np轨道杂化而得。sp2杂化轨道间的夹角为120°,呈平面三角形(如BF3)
②sp2杂化后,未参与杂化的一个np轨道可以用于形成π键,如乙烯分子碳碳双键的形成。
(3) sp杂化轨道——BeCl2分子的形成
①sp杂化轨道是由一个ns轨道和一个np轨道杂化而得。sp杂化轨道间的夹角为180°,呈直线形(如BeCl2)。杂化后的2个sp杂化轨道分别与氯原子的3p轨道发生重叠,形成2个σ键,构成直线形的BeCl2分子。
②sp杂化后,未参与杂化的两个np轨道可以用于形成π键,如乙炔分子中的C≡C键的形成
6.杂化轨道与分子空间构型
- 杂化轨道用于形成σ键或用来容纳未参与成键的孤电子对,
- 当没有孤电子对时,能量相同的杂化轨道彼此远离,形成的分子为对称结构;
- 当有孤电子对时,孤电子对占据一定空间且对成键电子对产生排斥,形成的分子的空间结构也发生变化。
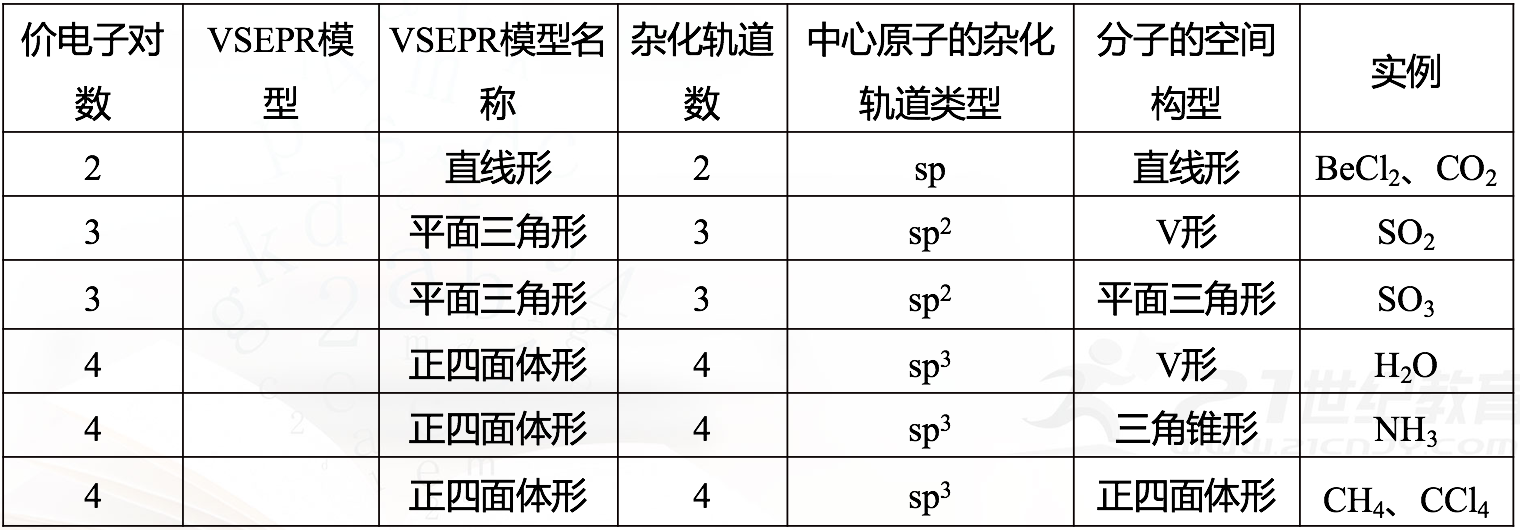
杂化轨道与分子的空间结构的关系
【讨论交流】分析CO2、SO2、SO3、H2O、NH3、CH4的杂化轨道类型、VSEPR模型、空间构型,总结VSEPR模型与中心原子的杂化轨道类型的关系。
【思考】用杂化轨道理论解释NH3、H2O的空间结构。
- 当杂化轨道中有未参与成键的孤电子对时,由于孤电子对参与互相排斥,使分子的空间结构与杂化轨道的形态发生变化。
- 如水分子的氧原子的sp3杂化轨道中有2个被孤电子对占据,其分子不呈正四面体形,而呈V形;
- 氨分子的氮原子的sp3杂化轨道中有1个被孤电子对占据,氨分子不呈正四面体形,而呈三角锥形。
中心原子轨道杂化类型的判断
- 根据杂化轨道的立体构型判断若杂化轨道在空间的分布为正四面体形或三角锥形,则分子的中心原子发生sp3杂化②若杂化轨道在空间的分布呈平面三角形,则分子的中心原子发生sp2杂化。③若杂化轨道在空间的分布呈直线形,则分子的中心原子发生sp杂化。
- 根据杂化轨道之间的夹角判断若杂化轨道之间的夹角为109°28′,则分子的中心原子发生sp3杂化;
- 若杂化轨道之间的夹角为120°,则分子的中心原子发生sp2杂化;
- 若杂化轨道之间的夹角为180°,则分子的中心原子发生sp杂化。
- 根据等电子原理进行判断如CO2是直形线分子,CNS-、N3-与CO2互为等电子体,所以分子构型均为直线形,中心原子均采用sp杂化。
- 根据中心原子的价电子对数判断中心原子的价电子对数为4,是sp3杂化
- 根据分子或离子中有无π键及π键数目判断如没有π键为sp3杂化,含1个π键为sp2杂化,含2个π键为sp杂化。
【思考与讨论】CH4、NH3、H2O中心原子的杂化类型都为sp3,键角为什么依次减小?从杂化轨道理论的角度比较键角大小时有什么方法?
- CH4、NH3、H2O中心原子都采取sp3杂化,中心原子的孤电子对数依次为0个、1个、2个。
- 由于孤电子对对共用电子对的排斥作用使键角变小,孤电子对数越多排斥作用越大,键角越小。
- 比较键角时,先看中心原子杂化类型,杂化类型不同时:一般键角按sp、sp2、sp3顺序依次减小;杂化类型相同时,中心原子孤电子对数越多,键角越小。
【课堂练习】
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
1.价电子对之间的夹角越小,排斥力越小。 ( )
2.NH3分子的VSEPR模型与分子空间结构不一致。( )
3.五原子分子的空间结构都是正四面体形。( )
4.杂化轨道与参与杂化的原子轨道的数目相同,但能量不同。( )
5.凡是中心原子采取sp3杂化轨道成键的分子,其空间结构都是正四面体形。( )
6.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键。( )
答案: (1)× (2)√ (3)× (4√) (5) ×
2.2.根据价层电子对互斥模型及原子杂化轨道理论判断NF3分子的空间结构和中心原子的杂化方式为( )
A.直线形 sp杂化
B.平面三角形 sp2杂化
C.三角锥形 sp2杂化
D.三角锥形 sp3杂化
答案:D。判断分子的杂化方式要根据中心原子的孤电子对数以及与中心原子相连的原子个数。在NF3分子中N原子的孤电子对数为1,与其相连的原子数为3,根据原子杂化轨道理论可推知中心原子的杂化方式为sp3杂化,NF3分子的空间结构为三角锥形,类似于NH3。
3.在BrCH=CHBr分子中,C—Br键采用的成键轨道是( )
A.sp-p B.sp2-s
C.sp2-p D.sp3-p
答案:C。分子中的两个碳原子都是采取sp2杂化,溴原子的价电子排布式为4s24p5,4p轨道上的一个未成对电子与碳原子的一个sp2杂化轨道成键。
4.指出下列原子的杂化轨道类型、分子的结构式及空间结构。
(1)CS2分子中的C为杂化, 空间结构为;
(2)CH2O中的C为杂化, 空间结构为;
(3)CCl4分子中的C为杂化, 空间结构为;
(4)H2S分子中的S为杂化, 空间结构为。
答案:轨道杂化所用原子轨道的能量相近,且杂化轨道只能用于形成σ键,未参与杂化的p轨道还可以形成π键。
(1)sp 直线型 (2)sp2 平面三角形 (3)sp3 正四面体 (4)sp3 V形
|
认真思考
思考
认真思考
主动探究
检测反馈
| 通过思考甲烷分子的形成过程,产生认知冲突。
认识杂化轨道理论。
通过认识杂化轨道理论,理解甲烷分子的形成过程。
通过对杂化轨道理论的学习,能从微观角度理解中心原子的杂化轨道类型对分子立体构型的影响。
通过对杂化轨道理论的学习,掌握中心原子杂化轨道类型判断方法,建立分子立体构型分析的思维模型。
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图