|
|
人教版九年级化学下册
《实验活动5常见金属的物理性质和化学性质》教学设计
【教材分析】
在第八单元中介绍了金属的物理性质和化学性质以及金属的冶炼和保护,本节课安排在第八单元之后旨在通过分组实验、讨论归纳,使学生进一步巩固和加深对金属物理性质的认识,巩固和加深对金属某些化学性质的认识。通过合作展示、分组实验、讨论归纳,掌握用设计实验来比较金属活动性强弱的方法,培养实验设计能力,并初步学会如何评价实验方案学情分析。
【学情分析】
学生在第二三单元学习了氧气和水的性质,对单个物质的物理性质和化学性质有所了解,第六单元学习了碳单质、一氧化碳和二氧化碳的性质,从而对含同种元素的物质的物理性质和化学性质有所了解。所以对于研究元素化合物的一般程序和方法都已不再陌生,但是学生仍缺乏设计实验和评价实验方案的能力。学生在第八单元中学习了金属的物理性质和化学性质,但只是观看教师的演示实验,并没有亲自动手去验证金属的性质。在本节课的学习中学生在知识层面上从零散到系统化,从能力层面上学生从了解实验事实到理解和应用。
【教学目标】
1.通过课前预习和课堂总结巩固和加深对金属颜色、硬度、导电性等物理性质以及金属与酸、金属与化合物溶液的反应等化学性质的认识。通过对铝制易拉罐和铁制易拉罐的探究实验,初步形成基本的化学实验技能和设计实验方案的能力。
2.通过实验探究以及对金属性质的认识,初步学会运用观察、实验等方法获取信息并用化学语言表达有关信息。
3.通过实验探究合作学习逐步形成认真细致、勤于动手的学习态度,初步感受科学探究的方法和对知识建构的重要意义,培养学生的环保理念。
【教学重点】
认识常见金属的化学性质。
【教学难点】
培养实验设计能力。
【教学方法】
实验学习法、探究学习法、合作学习法、引导探究、讲练结合
【教学准备】
- 教师准备:试管、试管夹、酒精灯、坩埚钳、电池、导线、小灯泡、
火柴。镁条、锌粒、铝片、铁片、铁粉、铜片、黄铜片(或白铜片)、稀盐酸、稀硫酸、硫酸铜溶液、硝酸银溶液。
【教学过程】
实验目的:
1.巩固和加深对金属性质的认识。
2.进一步提高实验设计能力。
实验用品:
试管、试管夹、酒精灯、坩埚钳、电池、导线、小灯泡、火柴。
镁条、锌粒、铝片、铁片、铜片、黄铜片(或白铜片)、稀盐酸、稀硫酸、硫酸铜溶液、硝酸银溶液。
你还需要的实验用品:铜丝、铁丝等。
【新课导入】我们已经学习了金属的物理性质和化学性质,今天我们将带着所学的理论知识,进行实验来感知金属的物理化学性质。引入新课。
【设计意图】温故知新。
【探究新知】
一、金属的物理性质
1.观察并描述镁、铝、铁、铜的颜色和光泽。
现象:镁、铝、铁均为有金属光泽的银白色固体,铜为有金属光泽的紫红色固体。
结论:金属具有金属光泽,镁、铝、铁等大多数金属都呈银白色,铜呈紫红色。
2.采取相互刻画的方法,比较铜片和铝片、铜片和黄铜片(或白铜片)的硬度。
现象:铝片表面有划痕;铜片表面有划痕。
结论:铝的硬度比铜小;铜的硬度比黄铜(白铜)小;
合金的硬度与组成它的纯金属不同,一般情况下合金
的硬度大于其组分金属的硬度。
3.请你设计并进行实验,证明金属具有导电性(或导热性、延展性)。
①导电性
设计实验:按图分别换用不同金属片连接电路。
实验现象:电路中灯泡亮。
结论: 金属具有导电性。
②导热性:
设计实验:剪一段金属,加热一端。
实验现象:另一端也能感受到变热。
结论: 金属具有导热性。
③延展性:
设计实验: 将一根铁丝在空气中持续加热至红炽,并在两端用镊子轻拉。
实验现象: 铁丝明显拉长。
结论: 金属具有延展性。
【总结金属的物理性质】:
1.金属都有光泽,大部分金属呈银白色,铜呈紫红色。
2.金属都具有导电性、延展性、导热性。
3.不同金属的硬度不同,合金的硬度大于组成成分金属的硬度。
巩固提升:
同学们经常喝易拉罐饮料,有的易拉罐是铝制的,有的易拉罐是铁制的,请你用物理性质区分它们。
方法一:可以取两个大小相近的易拉罐用手掂一掂,较轻的是铝制的,较重的是铁制的。
方法二:比较硬度,硬度大的是铁制的,硬度小易变形的是铝制的。
方法三:分别用磁铁吸引两个易拉罐,能被磁铁吸引的为铁制的,不能被吸引的为铝制的。
新知探究:
二、金属的化学性质
1.用坩埚钳夹取一块铜片,放在酒精灯火焰上加热,观察铜片表面的变化。
实验现象:紫红色的铜片变黑。
2Cu+O2 = 2CuO加热结论:铜与氧气在加热的条件下生成氧化铜。
2.向5支试管中分别放入少量镁条、铝片、锌粒、铁片、铜片,然后分别向各试管中加入约5mL稀盐酸(或稀硫酸),观察现象。填写表格并写出化学方程式。
结论:镁、铝、锌、铁、铜五种金属活动性顺序Mg>Al>Zn>Fe>(H)>Cu
Cu不能与酸反应置换出氢。
3.请你设计并进行实验,比较铁、铜、银的金属活动性强弱并填写表格
【金属的化学性质总结】:
1.铜与氧气在加热的条件下生成氧化铜。
2.镁、铝、锌、铁、铜五种金属活动性顺序Mg>Al>Zn>Fe>(H)>Cu
Cu不能与酸反应置换出氢。
3.排在前面的金属能够把后边的金属从化合物的溶液中置换出来。
巩固提升:
1.市面上的假黄金(Cu、Zn合金)与真黄金在外观上相似,请你根据金属的化学性质,用三种不同的方法鉴别真假黄金。
方法一:灼烧,若表面变黑则为假黄金;若表面不变化,则为真黄金。
方法二:放入稀硫酸中,若表面冒气泡,则为假黄金;若表面无变化,则为真黄金。
方法三:放入CuSO4溶液中,若表面变红色,则为假黄金,否则为真黄金。
2.铁是银白色金属。在上述实验中,你观察到的铁片和铁粉是什么颜色的?你发现了什么问题?查阅资料,与同学交流。
因为铁粉比较细,光学原因造成漫反射,只有很少的光进入我们的眼睛,所以铁粉显黑色。
【课后小结】
课堂小结:
物理性质:
1.金属都有光泽,大部分金属呈银白色,铜呈紫红色。
2.金属都具有导电性、延展性、导热性。
3.不同金属的硬度不同,合金的硬度大于组成成分金属的硬度。
化学性质:
1.铜与氧气在加热的条件下生成氧化铜。
2.镁、铝、锌、铁、铜五种金属活动性顺序Mg>Al>Zn>Fe>(H)>Cu
Cu不能与酸反应置换出氢。
3.排在前面的金属能够把后边的金属从化合物的溶液中置换出来。
【板书设计】
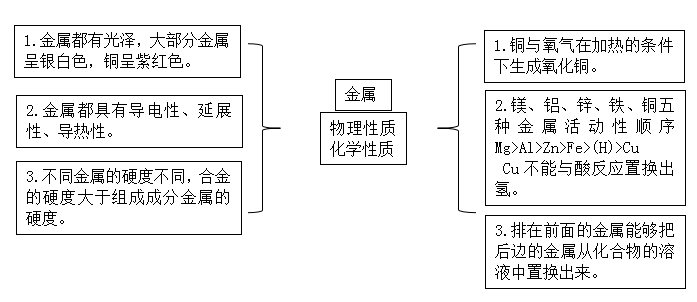
【课后作业】
总结实验中遇到的问题并写出解决方案。
【教学反思】
亮点:学生对金属这一章节的基础知识掌握不太扎实,整体实验操作能力一般,部分学生有较好的实验习惯,善于思考,学习热情高,上课大多数学生能积极回答问题。这节课是学生在初步学习了金属的物理性质和某些化学性质的基础上开展的实验教学,通过学生的亲手实验操作巩固和加深学生对金属性质的认识,锻炼了学生实验设计能力。希望通过本节课使学生的实验能力进一步得到提高,培养学生的科学探究精神。
不足:以学生的探究活动为主,在活动中用问题引导学生进行思考,充分发挥学生的主体地位。
- 教学建议:以后的教学,更多的使用小组合作抓住学生,运用探究式的教学方法,充分调动学生的积极性。
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图