| 本节课将通过探究活动,引导学生从离子的角度初步理解中和反应的原理,掌握其本质,为后续高中阶段的化学学习奠定基础。此外,学生已有了一定的分析推理能力,对于生活中中和反应的应用,只需在教师的引导下,通过自主学习来加深理解。这一过程不仅可以激发学生的学习兴趣,还能进一步培养他们的学习能力和创造力。
|
教学目标
| 1.通过实验探究,认识酸和碱的中和反应,学会运用指示剂判断反应的发生。
2.能从微观角度了解中和反应的原理,初步了解盐的概念,并会正确书写中和反应的化学方程式。
3.能够分析中和反应过程中溶液pH的变化情况。
4.了解中和反应在实际生活中的应用,认识化学与人类生产、生活的密切关系。
|
教学重、难点
| 重点:中和反应及其应用。
难点:从微观角度初步认识酸碱中和反应。
|
核心素养
| 化学观念:理解酸碱中和反应的实质,构建科学的化学观念。
科学思维:培养分析和推理能力,形成严谨的科学思维方式。
科学探究与实践:通过实验提升动手能力和探究能力。
科学态度与责任:增强团队合作精神,认识化学在生活中的重要性,提升责任感。
|
教学过程
|
教学环节
| 教学活动
| 设计意图
|
| 【知识回顾】酸的性质和碱的性质。
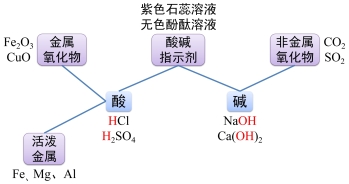
【问题引入】酸和碱之间能发生反应吗?
【实验探究】用两支试管分别取少量的稀盐酸和氢氧化钠溶液,一起倒入小烧杯中,搅拌,并观察现象。
【交流讨论】观察到什么现象?据此现象能否判断盐酸和氢氧化钠溶液发生了化学反应?
| 帮助学生回忆酸和碱的性质,用开放性问题激发学生的好奇心,引导他们思考
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图