|
|
第2课时 碳的化学性质
【学习目标】
1.了解常温下碳的稳定性。
2.掌握不同条件下碳与氧气的反应。
3.掌握碳与某些氧化物的反应,认识碳的还原性。
【学习重点】掌握单质碳的化学性质,理解碳的还原性的实质和还原反应的含义。
【学习难点】理解碳的还原性的实质、还原反应的实质和还原反应的含义。
【学习过程】
一、自主学习
1.碳的单质在常温下化学性质不活泼。
二、新知导学
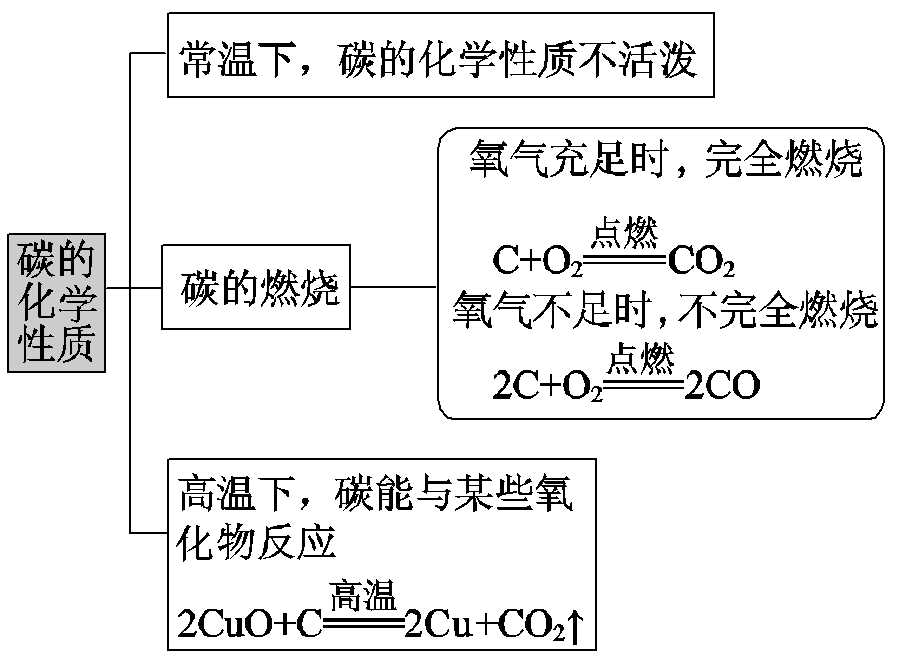
知识点一:碳的化学性质
【引导自学】阅读课本P110,请概括出碳的化学性质。
1.常温下,碳的化学性质不活泼。 从原子结构的角度分析,碳原子核内质子数为6,原子结构示意图为
,最外层有6个电子,化学性质不活泼。
2.碳的可燃性
3.碳的还原性:木炭还原氧化铜的实验探究
【师生合作】观察教师演示P107实验6-2,并记录实验现象。
实验装置
| 实验现象
| 实验结论
|
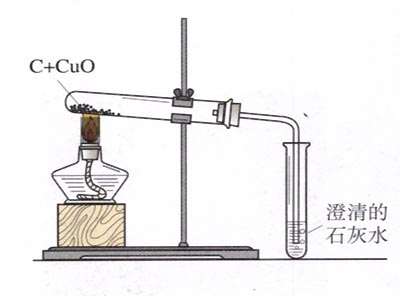
| 黑色粉末变为光亮的红色
| 说明生成了铜,在反应中,氧化铜被还原,失去氧
| | 澄清石灰水变浑浊
| |
【小组讨论】围绕上述实验,回答相关问题:
1.实验中在酒精灯上加一个金属网罩的作用是使火焰集中,提高温度。
2.将碳和氧化铜粉末混合均匀的目的是增大反应物的接触面积,提高反应速率。
3.停止加热时,应先将导管从溶液中拿出,再熄灭酒精灯。
4.实验结束后,应待试管冷却后才能将试管里的粉末倒出,防止热的铜被氧化为氧化铜。
5.碳和金属氧化物反应的规律:C + 金属氧化物金属+ CO2。
三、我的收获
四、当堂检测
1.古代字画能长期保存,是由于单质碳在常温下具有( A )
A.稳定性 B.氧化性 C.还原性 D.助燃性
2.一定质量的木炭与过量的氧气在密闭的容器内加热使其充分反应。如图中能正确反映容器内有关的量随时间变化的关系图象是( C )
A B C D
3.用木炭还原氧化铜的实验如左下图。
(1)酒精灯加灯罩的目的使火焰集中,提高温度;
(2)刚开始预热,试管②中立即产生气泡,但石灰水不变浑浊,原因是试管①中的空气受热膨胀进入试管②中,产生气泡;
(3)继续加热,观察到石灰水逐渐变浑浊,黑色粉末中出现红色物质。请你写出带点部分的化学方程式:
(4)停止加热时,应先将导管从试管②中撤出,并用弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末倒出。这样操作的原因是防止石灰水倒吸,防止热的铜被氧化为氧化铜。
五、布置作业
完成《学练优》本课时对应练习,并预习下一节的内容。
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图