课题3 二氧化碳的实验室制取
| 课时
| 2
| 授课年级
| 初三
|
课标要求
| 内容要求:
1.初步学习运用简单的装置和方法制取某些气体。
2.初步学习二氧化碳的实验室制法,归纳实验室制取气体的一般思路与方法。
3.学生必做实验及实践活动:二氧化碳的实验室制取。
学业要求:能设计简单实验,制备并检验二氧化碳。
|
教材
分析
| 本课题主要研究实验室里如何制取二氧化碳。教科书首先给出了实验室里制取二氧化碳的化学反应原理,然后探究实验室里制取二氧化碳的装置,最后总结实验室里制取气体的一般思路和方法。
探究实验室里制取二氧化碳的装置,是本课题的教学重点和难点,也是发展“科学探究与实践”素养的重要载体。该探究活动设计为问题、方案设计、评价与反思三个环节,其设计思路如下图所示。
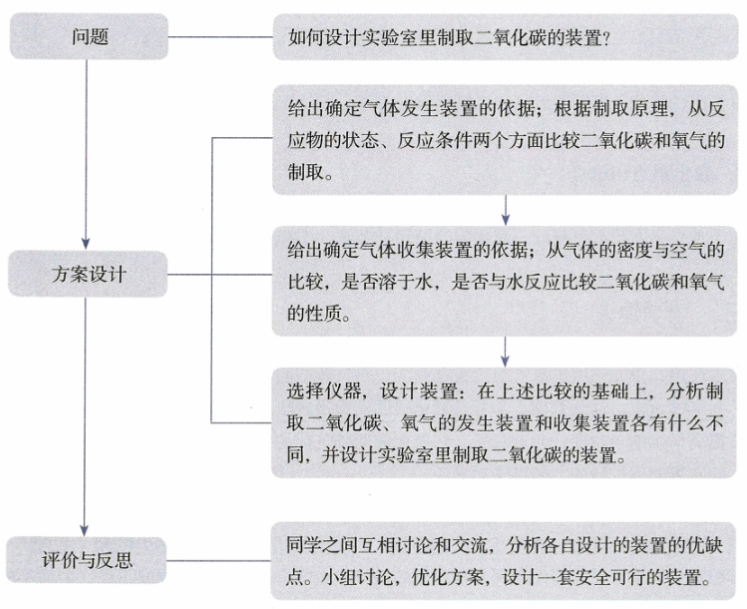
该探究活动在设计时,注重科学探究的核心要素显性化,目的是引导学生了解科学探究的一般过程,认识科学探究各要素之间的关系,发展学生科学探究的能力。
在探究活动之后,教科书给出了实验室里制取二氧化碳常用的一种装置(如教科书图6-19),供学生参考。然后,以“思考与讨论”栏目引出检验二氧化碳和证明二氧化碳是否集满的方法。
|
学情分析
| 学生在第二单元学习了氧气的实验室制法,对气体的制取原理、装置、收集、检验和验满等都有了一定的认识。在此基础上学习二氧化碳的实验室制法,应通过开放性的问题,运用多种教学手段提高学生的参与度。另外,教师要考虑到虽然学生对化学尤其是化学实验充满兴趣,但由于学生接触化学的时间不长,实验动手能力和分析能力还较弱,还不具备自主的实验探究能力,所以学习过程中,需要教师进行适当的点拨引导。
|
教学目标
| 1.了解实验室里制取二氧化碳的原理,学习比较、分析、归纳等科学方法。
2.探究实验室里制取二氧化碳的装置,学会依据探究目标设计并实施实验方案,体会合作与交流在科学探究中的重要作用。
|
教学重、难点
| 重难点:实验室制取二氧化碳的原理和装置。
|
核心素养
| 化学观念:通过对二氧化碳制取原理的探究,认识“在一定条件下通过化学反应可以实现物质转化”。
科学思维:通过对比、分析、归纳的思维过程推理出实验室制取二氧化碳时选取的发生装置和收集装置,并总结气体制取选取发生装置和收集装置的依据。
科学探究与实践:通过对实验室制取二氧化碳的探究,分析制取气体过程中装置的选取和实验操作的注意事项等,发展学生确定实验原理、选择实验仪器、组装实验装置等化学实验探究的能力。
科学态度与责任:通过了解二氧化碳的实验室制取方法,发展对物质世界的探究欲,保持对化学学习和科学探究的浓厚兴趣,对化学学科促进人类文明和社会可持续发展的重要价值具有积极的认识。
|
教学过程
|
教学环节
| 教学活动
| 设计意图
|
环节一、
新课导入
| 【图片展示】水草缸、二氧化碳灭火器、实验室探究二氧化碳性质装置。
【讲解】人类的生活、生产中会经常用到二氧化碳,如水草缸,即以水草为主题的水族缸,水草生长需要进行光合作用,光合作用必须有二氧化碳的参与,而水草缸中的水是死水,无法像自然界中的活水不断提供二氧化碳,因此需要透过二氧化碳供应系统来补充水中二氧化碳的浓度;二氧化碳灭火器中充装的是液态的二氧化碳,灭火时,二氧化碳从储存容器中喷出时,会由液体迅速汽化成气体,二氧化碳气体可以排除空气而包围在燃烧物体的表面或分布于较密闭的空间中,降低可燃物周围或防护空间内的氧浓度,产生窒息作用而灭火。且二氧化碳汽化时从周围吸收部分热量,起到冷却的作用。另外,在实验室探究二氧化碳的性质也需要一定量的二氧化碳。
【问题】那么工业上或实验室该如何制取CO2呢?
【交流讨论】上述反应原理是否同样适用于实验室制取CO2呢?
【总结】该反应所用试剂为石灰石,来源广,价格低。但反应条件为“高温”,要求较高,不易实现。所以该反应不适用于实验室制取CO2。
【过渡】那么实验室制取CO2的原理是什么呢?今天我们就来探究一下实验室中二氧化碳的制取吧!
| 通过生活、生产或实验室场景中需要用到二氧化碳引入二氧化碳的制取,然后再由工业制取原理进阶到实验室制取原理,使学生明确学习气体制取方法的必要性和原理选择的重要性
|
环节二、
实验室制取CO2的化学反应原理
| 【交流讨论】联系所学知识和日常生活,列举你所知道的能生成CO2的反应。
(1)生物体的呼吸作用可产生CO2
【思考】根据试剂选择的原则想一想,这些方法中哪些适用于实验室制取的二氧化碳?
【总结】反应(1):呼出的气体中除了有二氧化碳,还有氮气等其他气体,不纯净;反应(2)和(3):蜡烛或木炭在氧气中燃烧产生二氧化碳,若燃烧不充分还可能产生一氧化碳,产生的气体不纯净;反应(4):反应条件是高温,条件要求高,不易操作;反应(5)和(6):反应物中CO也是气体,会混入生成物中,造成气体不纯净。所以以上六个反应都不适合用于实验室制取二氧化碳。
【查阅资料】可以产生二氧化碳的反应。
(1)碳酸钠与稀盐酸反应:Na2CO3+2HCl = 2NaCl+H2O+CO2↑
(2)碳酸钠与稀硫酸反应:Na2CO3+ H2SO4 = Na2SO4+H2O+CO2↑
(3)石灰石与稀盐酸反应:CaCO3+2HCl = CaCl2+H2O+CO2↑
(4)石灰石与稀硫酸反应:CaCO3+H2SO4 = CaSO4+H2O+ CO2↑
【分析】上述四种反应,反应条件都是常温,反应较易进行,且只生成一种气体,产物纯净。
【问题】那么这些反应都适于实验室制取二氧化碳吗?下面通过以下实验探究的资料分析实验原理是否可行。
生成CO2的反应
| 实验现象
| 是否适用于实验室制取
| 1.碳酸钠粉末+稀盐酸/稀硫酸
| 剧烈反应,迅速产生大量气泡
| ×
| 2.碳酸钙粉末+稀盐酸/稀硫酸
| | | 3.块状石灰石+稀盐酸
| 产生气泡,速率适中
| √
| 4.块状石灰石+稀硫酸
| 刚开始有少量气泡产生,一段时间后反应停止
| ×
|
【分析】实验1、2:反应的速率太快,产生的气体不利于收集,故不便采用;实验4虽然开始会产生二氧化碳,但由于生成的硫酸钙是微溶物质,会覆盖在大理石的表面,阻碍反应进一步进行。故也不便采用;实验3操作简便,原料廉价,反应速率适中,气体易于收集,反应条件易于控制且生成物无杂质。故实验室通常选用大理石(或石灰石)与稀盐酸反应来制取二氧化碳。
【总结】有二氧化碳生成的化学反应很多,但不一定都适用于实验室制取二氧化碳,这里首先要考虑可操作性,在可操作的前提下,再考虑哪个更方便易行、原料是否易得、反应是否可控、是否利于收集等。
【讲解】实验室制取二氧化碳的反应物是石灰石(或大理石)和稀盐酸,石灰石(或大理石)的主要成分是碳酸钙;稀盐酸的主要成分是氯化氢和水,石灰石或大理石中的碳酸钙与稀盐酸中的氯化氢反应,生成氯化钙和碳酸,CaCO3+2HCl=CaCl2+H2CO3,碳酸不稳定,很容易分解成二氧化碳和水,H2CO3 =H2O+CO2↑。将第一个反应式中的碳酸用水和二氧化碳加以替换,这样,就得到了该反应的总的化学方程式:CaCO3+2HCl= CaCl2+H2O +CO2↑。
【对应训练】下列化学反应可用于实验室制取二氧化碳的是( )
A.木炭燃烧
B.人体的呼吸作用
C.石灰石与稀盐酸反应
D.高温煅烧石灰石
【答案】C
| 通过讨论、分析、资料等内容使学生逐步深入了解实验室制取气体时,选取反应原理应考虑的因素,
培养学生分析问题的能力和证据推理能力,并让学生掌握实验室制取气体的反应原理确定原则
|
环节三、
实验室制取CO2的装置
| 【知识回顾】实验室制取O2的思路。
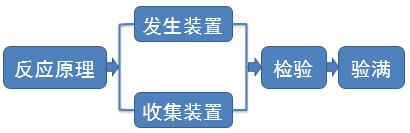
【过渡】确定了气体的制取原理之后,还需要确定制取气体的实验装置、实验操作和气体的检验、验满等。
【交流讨论】回顾实验室制氧气的原理和装置,分析确定气体的发生装置和收集装置时应考虑哪些因素?
【总结】实验室制取气体的装置一般分为发生装置和收集装置两部分,确定气体的发生装置要考虑两个因素:(1)反应物的状态:是固体与固体反应;还是固体与液体反应;还是液体与液体反应;(2)反应条件:是否需要加热;是否需要催化剂。确定气体的收集装置要依据气体的性质,根据密度和是否与空气成分反应确定排空气法,根据溶解性和是否与水反应确定排水法。
【学生活动】二氧化碳和氧气的实验室制取及相关性质比较——确定发生装置。
| 制取原理
| 反应物的状态
| 反应条件
| CO2
| 稀盐酸与大理石(或石灰石)
| 固体+液体
| 常温
| O2
| 加热高锰酸钾
| 固体
| 加热
| | 分解过氧化氢溶液
| 液体
| 常温、二氧化锰作催化剂
|
【总结】加热高锰酸钾制取氧气,反应物都是固体,反应都需要加热,故使用固体加热型发生装置,而分解过氧化氢溶液制氧气,反应物是液体,反应不需要加热,催化剂为固体,故使用固液常温型发生装置。实验室用稀盐酸与大理石或石灰石反应制取二氧化碳,反应物为固体和液体,反应不需要加热,故应使用固液常温型发生装置。
【学生活动】二氧化碳和氧气的实验室制取及相关性质比较——确定收集装置。
| 气体的密度与空气的比较(大或小)
| 是否溶于水,
是否与水反应
| 收集装置
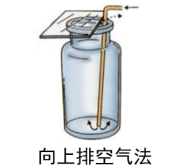
| CO2
| 大
| 溶于水,与水反应
|
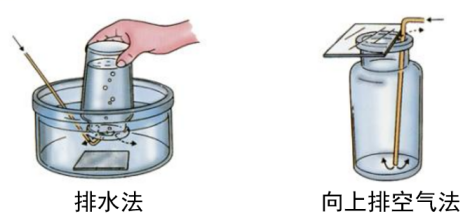
| O2
| 大
| 不易溶于水,不与水反应
|
|
【总结】实验室收集二氧化碳用向上排空气法。
【学生活动】选择以下实验仪器,小组合作组合一套制取二氧化碳的装置并介绍装置的特点。
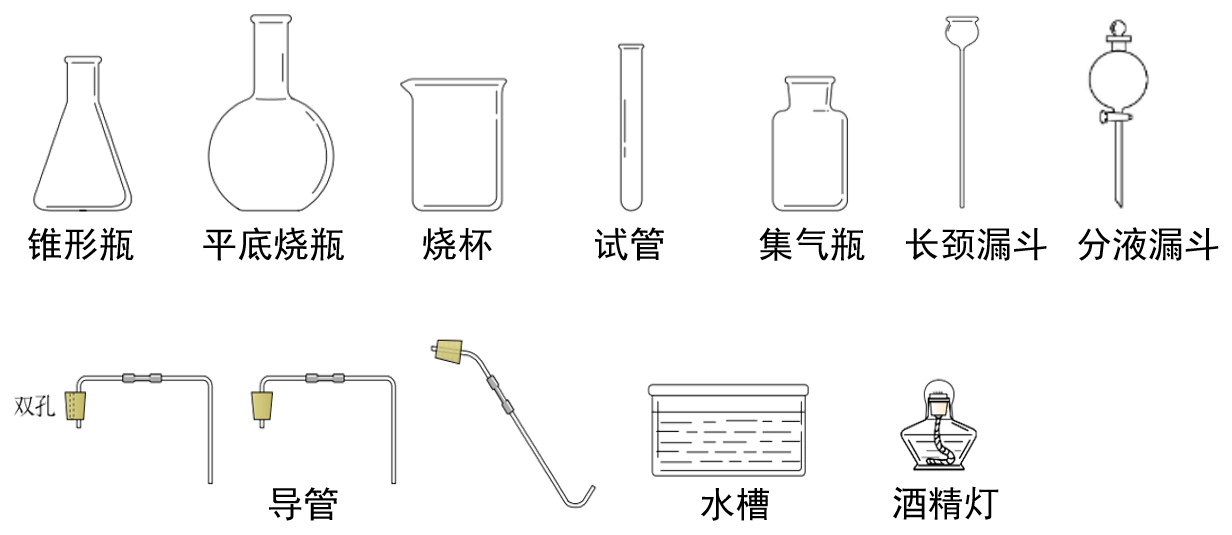
【提示】长颈漏斗和分液漏斗都是用于添加液体试剂的仪器,其中分液漏斗有活塞,可以控制液体试剂的滴加量和滴加速度。
【总结】
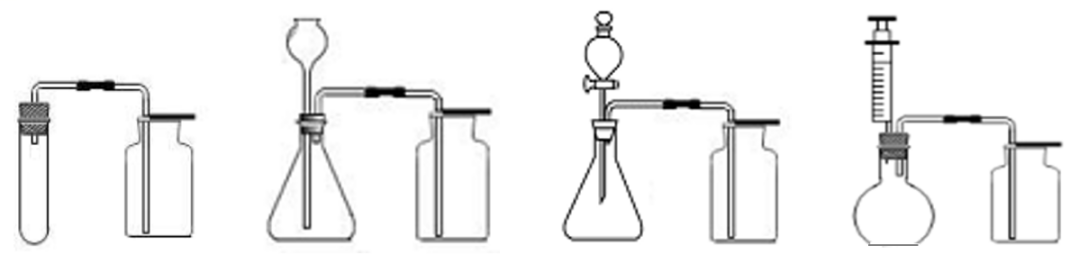
装置①操作简便,但由于试管容积小,所以一次性添加药品的量少,产生的气体少,适于制取少量气体;装置②③④容积大,而且可以多次添加液体药品,产生气体的量大,还方便随时添加液体药品;装置③④还可以通过控制添加液体的量从而控制产生气体的量,通过控制滴加液体的速率,在一定程度上也能控制反应的速率。
【过渡】依据实验室制取气体的思路,除了要确定反应原理和实验装置外,还要对制取的气体进行检验和验满。那么如何检验收集的气体为二氧化碳呢?用集气瓶收集二氧化碳时,怎样证明集气瓶中已充满了二氧化碳?
【总结】二氧化碳的检验和验满依据的都是二氧化碳的性质。
(1)二氧化碳的检验:将气体通入到澄清石灰水中,若石灰水变浑浊,则气体为CO2。依据是二氧化碳能使澄清石灰水变浑浊。
(2)二氧化碳的验满:将燃着的木条放在集气瓶口,若木条熄灭,则CO2已满。依据是二氧化碳既不可燃,也不支持燃烧。
【学生活动】观看实验室制取二氧化碳的视频或教师演示实验,总结实验室制取二氧化碳的操作步骤。
【总结】实验室制取二氧化碳的操作步骤:
【交流讨论】
1.长颈漏斗下端管口为什么要伸入液面以下?(防止气体从长颈漏斗排出。)
2.集气瓶内的导管为什么要伸入到接近集气瓶底部?(排尽集气瓶内的空气,以收集到更纯的二氧化碳。)
【对应训练】
1.下列制取、收集、验满、检验CO2的装置和原理能达到实验目的的是( )
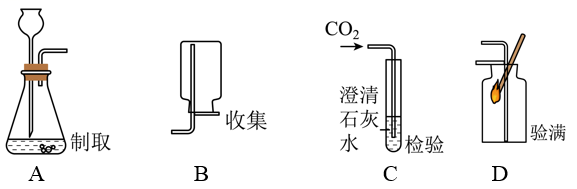
2.如图是实验室的部分实验装置,回答有关问题:
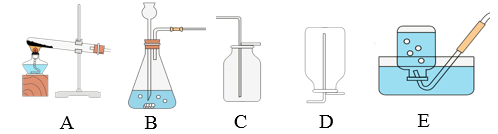
(1)实验室用稀盐酸与石灰石反应制取二氧化碳应选用的装置是________(填序号);其中,发生装置中产生二氧化碳的化学方程式为_________________________________。
(2)检验二氧化碳是否集满的方法:________________________________。
【答案】1. C
2.(1)BC CaCO3+2HCl == CaCl2+H2O+CO2↑
(2)将燃着的木条放在集气瓶口,观察木条是否熄灭
| 通过与实验室制取O2的思路作对比,引导学生设计实验室制取二氧化碳的装置,建构实验室里制取二氧化碳的思路和方法,培养学生的高级思维
能力
|
课堂总结
|
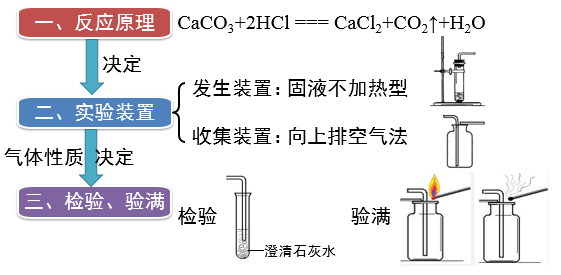
|
板书
设计
| 课题3 二氧化碳的实验室制取
第1课时 实验室制取二氧化碳
一、反应原理
石灰石或大理石、稀盐酸:CaCO3+2HCl=CaCl2+H2O+CO2↑
二、实验装置
发生装置:固液常温型
收集装置:向上排空气法
三、CO2的检验
通入澄清石灰水——变浑浊
四、CO2的验满
燃着的木条放在集气瓶口——熄灭
|
教学
反思
| 本课时的内容一方面是学习二氧化碳的实验室制法,另一方面是渗透实验室制取气体的一般思路和方法。所以在授课时要采用讨论、分析、自主探究等形式进行,以便学生理解选择气体制取原理和装置背后的逻辑。
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图