课题2 碳的氧化物
| 课时
| 2
| 授课年级
| 初三
|
课标要求
| 内容要求:
跨学科实践活动:基于碳中和理念设计低碳行动方案
学业要求:
能基于物质的性质和用途,从辩证的角度,初步分析和评价物质的实际应用,对空气保护、低碳行动等社会性科学议题展开讨论,积极参与相关的综合实践活动。
|
教材
分析
| 本课题主要介绍了二氧化碳、一氧化碳的性质和用途,以及温室效应、低碳行动与可持续发展等内容。
关于二氧化碳,教科书首先通过【实验6-3】【实验6-4】和【实验6-5】,分别介绍了二氧化碳的性质:密度比空气的大,不能燃烧,不支持燃烧;能溶于水;与水发生化学反应等。然后联系学生已有知识,介绍了二氧化碳能使澄清石灰水变浑浊的原因。最后介绍二氧化碳对生活和环境的影响。其中,二氧化碳与水的反应是本课题教学难点。
本课题的实验较多,目的是引导学生通过实验、观察,初步掌握对事实进行归纳概括、分析综合等科学方法,发展基于实验事实进行证据推理的思维能力,在此基础上建构认识物质性质的一般思路与方法。
本课题在介绍二氧化碳的性质时,注意密切联系其用途。例如:二氧化碳不燃烧、不支持燃烧的性质可用于灭火;二氧化碳能溶于水的性质可用于生产汽水等碳酸饮料;干冰升华吸热,因此干冰可作制冷剂和用于人工增雨等。这样编写的目的是,引导学生认识物质性质在生活、生产、科技发展等方面的广泛应用,进一步强化学生对物质的性质和用途之间关系的认识。
|
学情分析
| 二氧化碳是初中化学中继氧气之后的又一种重要气体。该气体与日常生活联系非常紧密,学生在前期的学习中就有所接触,但对二氧化碳的性质和用途未必有科学的认识。例如怎样认识二氧化碳的“功”与“过”?另外,学生科学探究意识较为缺乏,看问题多停留于表面,缺乏深思的习惯。例如,当看到二氧化碳通入石蕊溶液中,石蕊溶液变红,他们就会得出二氧化碳能使石蕊溶液变红的错误结论。还有,CO2与CO都会致人死亡,但其原因是不同的,学生对CO2不能供给呼吸的性质和CO的毒性易混淆。
|
教学目标
| 1.通过实验探究认识二氧化碳的性质,加深对控制变量、对比实验、分析推理、归纳总结等科学方法的认识。
2.结合实例了解二氧化碳的用途,强化对物质的性质与用途之间关系的认识。
|
教学重、难点
| 重点:二氧化碳的性质和用途。
难点:二氧化碳与水的反应。
|
核心素养
| 化学观念:通过对二氧化碳性质和用途的学习,加深理解物质的性质决定用途。通过对二氧化碳和一氧化碳分子构成的比较,认识物质的多样性。
科学思维:通过运用比较、分析等科学方法,基于实验事实进行证据推理,推测二氧化碳的性质和用途,并能运用二氧化碳的性质解释和解决真实问题。
科学探究与实践:通过实验认识二氧化碳的物理性质和化学性质,发展学生的科学探究能力及与他人分工协作、沟通交流的能力。
科学态度与责任:通过对二氧化碳的性质和用途的学习和认识,发展学生对物质世界的好奇心、想象力和探究欲,保持对化学学习的浓厚兴趣。
|
教学过程
|
教学环节
| 教学活动
| 设计意图
|
环节一、
新课导入
| 【知识回顾】今天我们学习的课题是《碳的氧化物》,那么请同学们回顾一下,什么是氧化物呢?
【总结】氧化物:由两种元素组成,其中一种是氧元素的化合物。
【提问】那么碳的氧化物有哪些呢?请从宏观和微观角度分析这些氧化物。
【总结】碳的氧化物有两种,分别为一氧化碳和二氧化碳,从宏观角度分析:两种氧化物的元素组成相同,都是由碳元素和氧元素组成的;从微观角度分析:两种氧化物的分子构成不同,1个一氧化碳分子是由1个碳原子和1个氧原子构成,而1个二氧化碳分子是由1个碳原子和量个氧原子构成,两者的分子构成不同,所以两者的性质也不同。
【讲解】地球上生命的持续需要进行光合作用和呼吸作用,光合作用的原料是二氧化碳,而呼吸作用又产生二氧化碳,所以说二氧化碳是地球生命活动的基石。本节课我们来认识下二氧化碳的性质和用途。
| 通过物质的分类引入一氧化碳和二氧化碳,并从宏微两个角度分析碳的氧化物,使同学们认识物质的多样性以及物质的结构与性质的关系
|
环节二、
二氧化碳的性质和用途
| 【课件展示】水草缸、灭火器、汽水。
【讲解】二氧化碳也是生活中一种很常见的物质,它在人类的生产、生活中有非常广泛的用途,如图片所示,水草缸中持续通入二氧化碳以供给水草的光合作用,二氧化碳可用于灭火,冰爽美味的汽水的制造也与二氧化碳有关。
【过渡】根据前面的学习我们知道,物质的性质决定了物质的用途,物质的用途体现物质的性质,那么你能根据二氧化碳的这些用途推测出它有哪些性质吗?
【用途1】CO2作气体肥料
【提问】请说一说CO2作气体肥料的原因。
【讲解】CO2作气体肥料的原因是二氧化碳是植物光合作用的原料,在植物生长过程中补充二氧化碳,能促进植物的生长。

所以蔬菜大棚、水草缸中都会设置二氧化碳发生器,这都是在施肥。
【用途2】灭火
【提问】CO2能用于灭火,那么二氧化碳能燃烧吗?能支持燃烧吗?二氧化碳的密度应比空气大还是小呢?如何验证你的推测?
【实验验证1】将二氧化碳慢慢倒入放有高低不同位置的两支燃着的蜡烛的烧杯中,观察现象并分析。

【学生活动】观看实验视频或教师演示实验,观察并分析实验现象。
【总结】
现象
| 烧杯中燃着的蜡烛自下而上依次先后熄灭
| 分析
| 二氧化碳不能燃烧也不支持燃烧,而且密度比空气大,倾倒时先聚集到烧杯底部,使下方的蜡烛首先接触到较多的二氧化碳而熄灭,上面的蜡烛后接触到二氧化碳后熄灭
| 结论
| 1.CO2密度比空气大;
2. CO2不能燃烧,也不支持燃烧
|
由于以上性质,二氧化碳常用于灭火,常见的有手提式二氧化碳灭火器等。
【学生活动】交流讨论:你还能想到其他方法来验证二氧化碳的密度比空气大吗?
【方法展示】
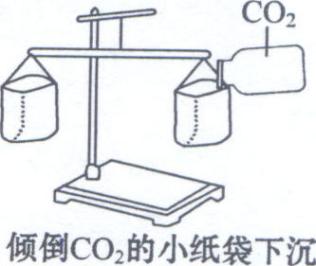
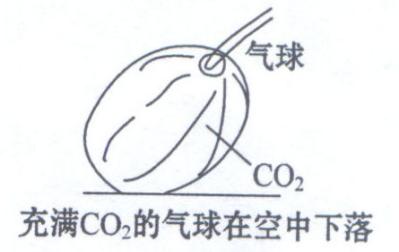
【拓展设问】氮气也不能燃烧,也不支持燃烧,为什么不用氮气灭火呢?
【总结】因为空气中氮气含量为78%,所以氮气的密度与空气相近,不能下沉到燃烧物的表面,不易灭火。
【用途3】制汽水
【图片展示】雪碧配料表。
【提问】在汽水的配料表中可以看到二氧化碳,二氧化碳常温常压下是无色无味的气体,而汽水呈液态,那么二氧化碳能溶于水吗?二氧化碳与水能反应吗?二氧化碳与水混合后液体性质变了吗?
【实验验证2】向一个收集满二氧化碳气体的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,振荡。观察现象并分析。
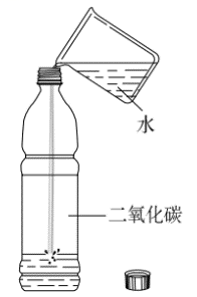
【学生活动】观看实验视频或教师演示实验,观察并分析实验现象。
【总结】
现象
| 塑料瓶变瘪了
| 结论
| CO2能溶于水
| 解释
| 部分CO2溶于水使瓶内气体减少,气压变小,大气压强使瓶子变瘪
|
二氧化碳能溶于水,通常状况下,1体积的水约能溶解1体积的二氧化碳,增大压强会溶解更多。生产汽水等碳酸饮料就是利用了这一性质。
【交流讨论】汽水的生产原理我们已经知道,那为什么可乐、雪碧等饮料统称为“碳酸饮料”?“碳酸”是什么呢?CO2溶于水会发生化学反应吗?
【实验验证3】取三朵用石蕊溶液染成紫色的干燥的小纸花。第一朵纸花喷上水,第二朵纸花直接放入盛有二氧化碳的集气瓶中,第三朵纸花喷上水后,再放入盛有二氧化碳的集气瓶中,观察三朵纸花的颜色变化。【资料】石蕊是一种从地衣中提取的色素。石蕊溶于水配制成的紫色石蕊溶液,遇酸变成红色。
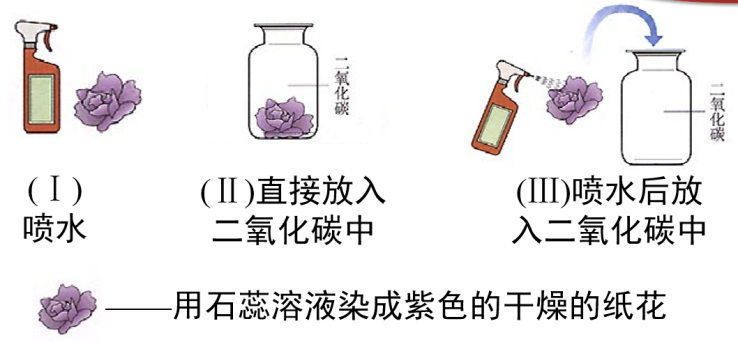
【学生活动】观看实验视频或教师演示实验,观察并分析实验现象。
【总结】
| (Ⅰ)喷水
| (Ⅱ)直接放入CO2
| (Ⅲ)喷水后放入CO2
| 现象
| 纸花不变色
| 纸花不变色
| 纸花由紫变红
| 分析
| 水不能使石蕊溶液变红
| CO2不能使石蕊溶液变红
| CO2与水反应生成酸性物质使石蕊溶液变红
| 结论
| CO2与水发生了化学反应
|
实验说明:CO2与水反应生成了酸性物质,即碳酸,碳酸能使紫色石蕊试液变成红色。
H2O+CO2=H2CO3
【演示实验】将上述实验的第四步得到的变红的小纸花,小心的用吹风机烘干,看到红色的纸花又变成了紫色。
【讲解】这说明了碳酸不稳定,受热易分解,即H2CO3=H2O+CO2↑。
【交流讨论】在炎热的夏季喝下冰凉的碳酸饮料后,除了凉爽之外,还会怎么样?
【总结】打嗝,原因就是碳酸受热分解造成的。
【提问】如何检验汽水中是否含有二氧化碳?
【总结】将气体通入到澄清的石灰水中,如果石灰水变浑浊了,则证明该无色无味的气体为二氧化碳。CO2 + Ca(OH)2 == CaCO3 ↓ + H2O,石灰水的主要成分是氢氧化钙,能与二氧化碳反应生成碳酸钙,碳酸钙难溶于水,则石灰水中会出现浑浊的现象,根据这个特殊的现象,该反应用于检验二氧化碳。
【交流讨论】工人师傅用石灰浆粉刷墙壁后,刚开始的一段时间内墙壁会“出汗”,你知道是什么原因吗?
【总结】原因是:CO2+Ca(OH)2=CaCO3↓+H2O。
【总结】二氧化碳的性质。
| 颜色
| 气味
| 密度
| 溶解性
| CO2
| 无色
| 无臭
| 比空气大
| 能溶于水
|
(1)不能燃烧,也不支持燃烧;
(2)能与水反应:H2O+CO2=H2CO3;
(3)能与氢氧化钙反应:CO2+Ca(OH)2=CaCO3↓+H2O。
【过渡】在加压和降温条件下,二氧化碳还可转变为液态、进而凝固为固态——“干冰”。
【讲解】干冰是固态的二氧化碳,除了用于低温保存食品外,还可用于营造舞台环境。另外还用于人工降雨,你知道这里面的原理是什么吗?
【学生活动】阅读教材,找出“干冰”用于人工降雨的原理。
【总结】干冰易升华吸热,使环境温度降低,将空气中的水蒸气凝结为小液滴,进而聚集成雨滴落下。
【讲解】通过学习我们知道,二氧化碳在生产、生活中有着广泛的用途,除了制作饮料,干冰用于人工降雨、人工云雾外,还有如下用途:光合作用、灭火、化工生产的原料、气体肥料等。
| 本节课先从物质“用途”的角度认识二氧化碳,再结合“物质的性质和用途的关系”通过设问引入二氧化碳的性质,然后通过实验验证,加深学生理解物质的性质和用途的关系,并使学生认识到实验对认识物质性质的重要作用
|
课堂练习
| 1.下列关于二氧化碳物理性质的叙述不正确的是( )
A.二氧化碳不能溶于水
B.通常情况下二氧化碳是无色无味的气体
C.固体二氧化碳俗称干冰,易升华
D.相同条件下,二氧化碳的密度比空气大
2.下列实验现象既能体现二氧化碳的物理性质,又能体现其化学性质的是( )
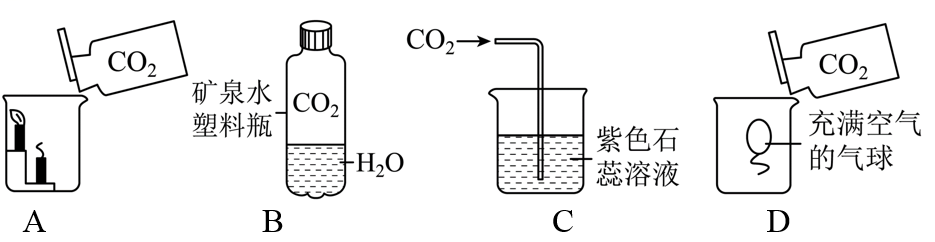
A.蜡烛自下而上熄灭 B.软塑料瓶变瘪
C.石蕊溶液变红 D.气球上浮
3.为探究二氧化碳能否和水反应,用三朵石蕊溶液染成紫色的干燥小花完成下图三个实验。实验Ⅰ、Ⅱ中小花不变色,实验Ⅲ中小花变红。下列说法不正确的是( )
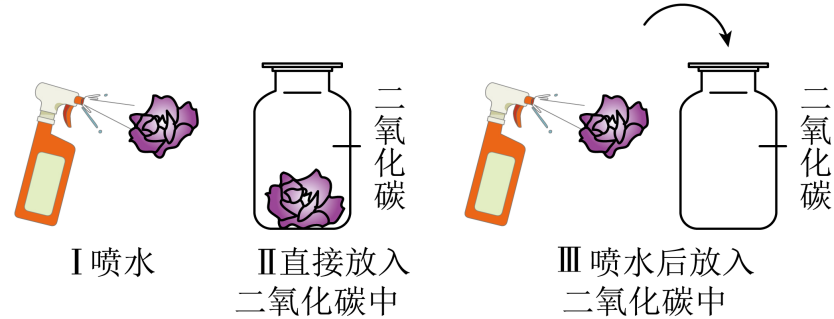
A.实验Ⅰ说明水不能使石蕊变红
B.实验Ⅱ说明二氧化碳不能使石蕊变红
C.仅凭实验Ⅰ和Ⅱ不能说明二氧化碳能与水发生化学反应
D.仅凭实验Ⅱ和Ⅲ就能说明二氧化碳能与水发生化学反应
【答案】1.A 2.A 3.D
|
课堂总结
|
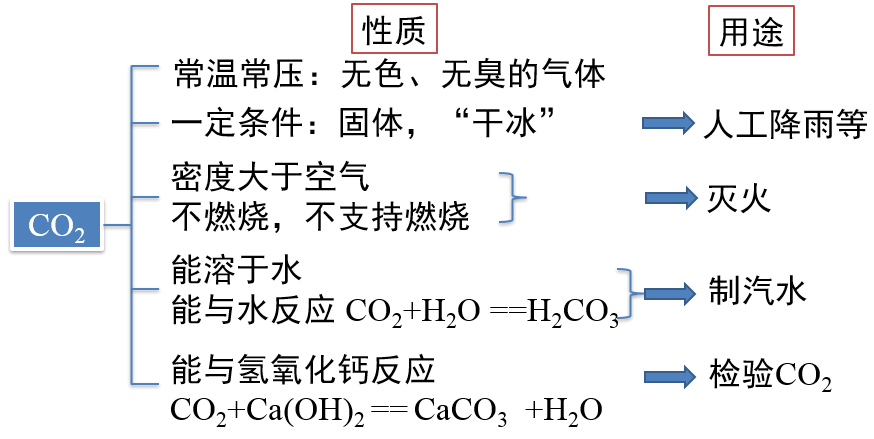
|
板书
设计
| 课题2 碳的氧化物
第1课时 二氧化碳的性质和用途
1.无色、无臭、气体
2.灭火 → 二氧化碳不燃烧,也不支持燃烧,密度比空气大
3.汽水 → 二氧化碳能溶于水且与水反应:CO2+H2O=H2CO3
4.CO2与澄清石灰水反应:CO2+Ca(OH)2=CaCO3↓+H2O → 检验二氧化碳气体
5.干冰 → ①制冷剂;②人工降雨。
|
教学
反思
| 本节课采用反向推导的设计思路,从用途的角度通过设问认识物质的性质,所以课堂中的设问非常重要,要留有学生思考的时间。
实验是认识物质的重要手段,本节课的实验设计进一步验证了这个说法。课堂中的实验设计要从学生的角度出发,多让学生观察、思考、提出问题等,发挥实验的真正作用。
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图