教学过程
|
教师活动
| 学生活动
|
新
课
导
入
| 思考探究:
说说下列符号所表示的含义:元素符号C和CO2
思考探究:
用化学式可以表示某种物质,那么,能不能用化学式来表示化学反应呢?
| 学生思考,自主探究,回答问题。
|
新知讲授
| 一、化学方程式
思考与讨论:用化学式可以表示某种物质,那么能不能用化学式来表示化学反应呢?
回答:可以
教师点拨:
化学方程式定义:用化学式来表示化学反应的式子叫化学方程式。
例如:
用化学式就可以表示为:
C + O2 CO2
这种用化学式来表示化学反应的方程式叫做化学方程式 (chemical equation)。上述方程式可读作“碳和氧气在点燃的条件下反应生成二氧化碳”。
思考与讨论:请比较上述两种化学反应的表示方式,你认为哪种方式可以更简便地表示化学反应的变化过程?
思考与讨论:化学式 CO2 具有多种意义,那么一个化学方程式是否也具有多种意义呢?
教师点拨:
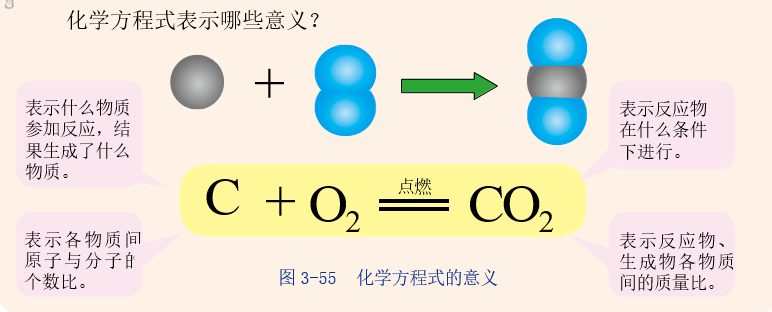
思考与讨论:怎样正确书写化学方程式呢?
教师点拨:
书写化学方程式的原则
1. 以客观事实为依据写出反应物和生成物
2. 要遵守质量守恒定律,即在式子左、右两边各原子的种类与数目必须相等。
3. 说明反应条件和生成物的状态。如果一个反应在特定的条件下 进行,如需点燃、加热 ( 通常用△表示 )、高温、通电、催化剂等,必 须把条件写在等号的上方或下方。 如果反应物中没有气体,而生成物中有气体产生,则在气体的化学式旁边用“↑”号表示;如果是溶液中发生的反应,反应物中无固体,而生成物中有固体的,则在固体的化学式旁边用“↓”号表示。例如:
2H2O =2H2↑+ O2↑
CO2 + Ca(OH)2 =CaCO3 ↓+ H2O

下面以磷在空气里燃烧生成五氧化二磷的反应为例,说明书写化学方程式的具体步骤:
1.根据反应事实,在式子的左边写出反应物的化学式,右边写出生成物的化学式,中间连一条短线。如果反应物或生成物不止一种,就分别用
“+”号连接起来。
P + O2 → P2O5
2.配平化学方程式。在式子左、右两边的化学式前面,要配上适当的
化学计量数,使式子两边每一种元素的原子总数相等。一般可用最小公倍数法来确定化学计量数。
4P + 5O2 → 2P2O5 式子两边各元素的原子数配平后,把短线改成等号。
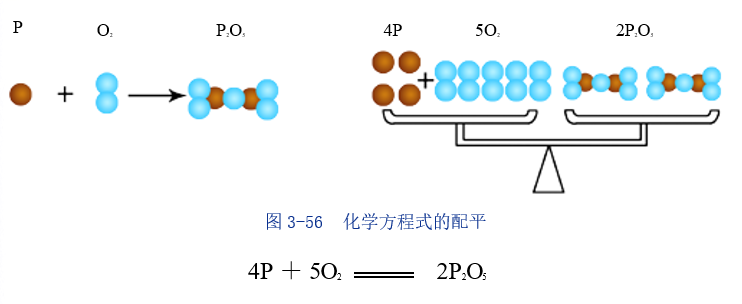
3. 思考与讨论:说说方程式的意义
教师点拨:

二、依据化学方程式进行计算
在工农业生产或科学研究中,常常要定量研究各物质间的质量关系。 例如,燃烧 2千克的木炭,至少需要消耗多少千克氧气;制取 2克氧气至少 需要分解多少克过氧化氢。如何来完成这些定量研究呢?
在上面的学习中,我们知道化学方程式可表示反应物、生成物各物质间的质量比。
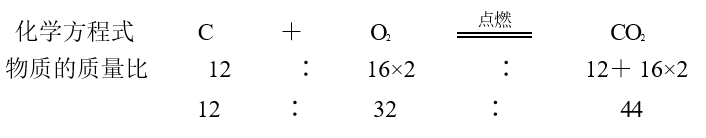
通过质量比我们可以知道每12份质量的 C 跟 32份质量的 O2 完全反应可生成44份质量的 CO2。
思考与讨论:现有24份质量的 C 能与多少份质量的 O2 完全反应?最后能生成多少份质量的CO2 ?
由于化学方程式能表示反应前后各物质的质量关系,因此我们可以利用化学方程式计算化学反应中各成分的质量。
[例题]实验室里用分解过氧化氢的方法制取氧气。现要制得2克氧气,至少需要多少克过氧化氢?

依据化学方程式计算的步骤一般为:

根据化学方程式计算的一般步骤
(1)设:根据题意设未知量
(2)写:书写正确的化学方程式
(3)找:找出相关物质的相对分子质量和已知
(4)列:列出比例式并求解
(5)答:检查结果,对问题做出简明回答
| 学生思考后回答。
学生思考。
学生观察后思考,用知识加以分析。
学生记录笔记。
学生记录笔记。
学生记录笔记。
|
课
堂
练
习
| 1.化学反应的实质是构成物质分子的原子重新进行组合,形成新分子的过程。如图是在密闭容器中某化学反应过程的微观变化示意图。据图回答正确的是( )
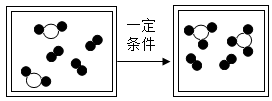
A.该反应生成了单质
B.该反应属于化合反应
C.反应前后分子和原子的种类与数目发生改变
D.参加反应的“”与“”的分子个数比为2:3
【答案】B
【解析】A、由微观反应示意图可知,该反应的生成物是一种化合物,故错误。
B、由微观反应示意图可知,该反应符合“多变一”的特征,属于化合反应,故正确。
C、由微观反应示意图可知,该反应前后原子种类和数量不变,故错误。
D、由微观反应示意图可知,参加反应的“”与“”的分子个数比为2:1,故错误。
故选B。
2.《本草纲目》中记载:“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸点燃药者。”该反应的原理为:2KNO3+S+3C=K2S+N2↑+3X↑。下列说法正确的是( )
A.生成物X的化学式是CO2 B.火药是纯净物
C.该反应过程中会吸收大量热 D.反应后氮元素的化合价升高
【答案】A
【解析】A、由反应前后原子种类和个数不变可知,X化学式为CO2,符合题意。
B、火药由多种物质组成,属于混合物,不符合题意。
C、该反应过程中会放出大量热,不符合题意。
D、反应后氮元素的化合价由+5变成0价,化合价降低,不符合题意。
故选A。
3.一定质量的某有机化合物完全燃烧,生成2.2gCO2和1.8gH2O,另取3.2g该有机化合物在O2中完全燃烧,消耗4.8gO2,该有机化合物的化学式可能是()
A.C2H4
B.CH4O
C.CH4
D.C2H4O
【答案】B
【解析】因为“一定质量的某有机化合物完全燃烧,生成2.2gCO2和1.8gH2O,另取3.2g该有机化合物在O2中完全燃烧,消耗4.8gO2”,由质量守恒定律可知,3.2g该有机化合物在O2中完全燃烧,消耗4.8gO2,同时生成4.4gCO2和3.6gH2O,该有机物中含碳元素的质量为:4.4g×<Object: word/embeddings/oleObject1.bin>×100%=1.2g;含氢元素的质量为:3.6g×<Object: word/embeddings/oleObject2.bin>×100%=0.4g;则其中含氧元素的质量为:3.2g-1.2g-0.4g=1.6g。则该有机物中,碳、氢、氧的原子个数比为:<Object: word/embeddings/oleObject3.bin> =1:4:1,所以化学式为CH4O。故选B。
|
课
堂
小
结
| 化学方程式是化学领域中一种重要的表达方式,它用化学式精确地描述了化学反应的过程。在书写化学方程式时,我们必须以实验事实为依据,确保方程式的正确性,并且需要符合质量守恒定律,即反应前后元素的原子个数必须保持相等。书写化学方程式的步骤包括写出正确的反应物和生成物化学式,通过配平确保方程式的平衡性,并注明反应条件和生成物的状态。化学方程式不仅代表了化学反应的过程,还承载着丰富的化学意义。在实际应用中,我们可以根据化学方程式进行计算,通过设定未知数、书写方程式、找出相关物质的相对分子质量和已知条件,列出比例式并求解,最后对结果进行简明的回答。这一计算过程为我们理解和量化化学反应提供了有力的工具。
|
板
书
设
计
| 一、化学方程式
1.化学方程式定义:用化学式来表示化学反应的式子叫化学方程式
2.书写原则
A、以客观事实为依据(反应是真实存在的,不能凭空臆造)
B、符合质量守恒定律。(反应前后两边各元素的原子个数必须相等)
3.书写步骤
(1)写出反应物和生成物的正确化学式。
(2)配平化学方程式。
在式子左、右两边每一种元素的原子数目必须相等。
(3)注明反应条件及生成物的状态。
4.化学方程式的意义
二、依据化学方程式进行计算
根据化学方程式计算的一般步骤
(1)设:根据题意设未知量
(2)写:书写正确的化学方程式
(3)找:找出相关物质的相对分子质量和已知
(4)列:列出比例式并求解
(5)答:检查结果,对问题做出简明回答
|
作
业
设
计
| |
反
思
评
价
| |
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图