教学过程
|
教师活动
| 学生活动
|
新
课
导
入
| 图片引入:
木头燃烧后只剩下灰烬,质量减少了。蜡烛燃烧后留下的蜡油很少,质量减少了。

问:化学变化后质量变小了?
问:化学变化后质量变大了?
问:真相究竟是什么?
| 学生思考,自主探究,回答问题。
|
新知讲授
| 一、质量守恒定律
思考与讨论:我们用过氧化氢制取氧气时,反应前后试管的总质量会如何变化?
如果把反应生成的氧气收集起来,加上氧气的质量,总质量又会如何变化?
当物质发生化学变化后,参加反应的反应物的总质量与生成物的总质量相比较,存在什么样的关系?
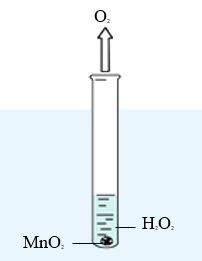
回答:反应前后质量相等
教师点拨:科学是基于实验证据的,所以接下我们进行几个实验。
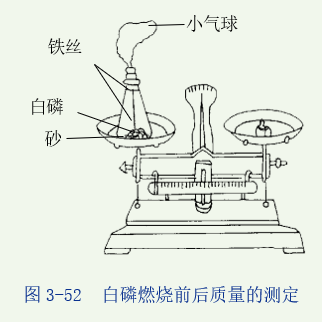
活动1:如图所示,将锥形瓶置于天平托盘上,调节平衡,取下锥形瓶,将瓶塞上的铁丝在酒精灯上烧红后,接触引燃白磷并立即塞紧瓶塞。待反应结束冷却后,重新放回天平托盘上,观察是否平衡。
回答:无数实验表明,反应前后物质的质量总和是相等的
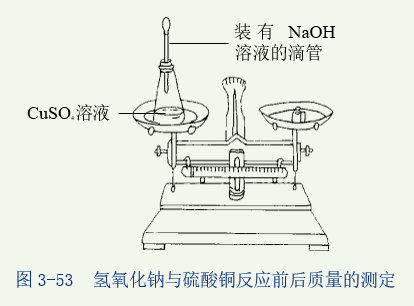
活动2:如图所示,将锥形瓶置于天平托盘上,调节平衡,然后取下锥形瓶,把滴管内的溶液滴入瓶内,使两种溶液混合,反应生成蓝色氢氧化铜,再将锥形瓶放回天平托盘上,观察是否平衡。
回答:无数实验表明,反应前后物质的质量总和是相等的
教师点拨:
质量守恒定律:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
思考:为什么物质在发生化学反应前后,各物质的质量总和相等呢?化学反应的实质是什么?请磷和氧反应生成五氧化二磷为例用分子和原子的知识加以分析。
回答:
反应物的原子种类和总数 生成物的原子种类和总数
磷原子 4个 磷原子 4个
氧原子 10个 氧原子 10个
原子总数 14个 原子总数 14个
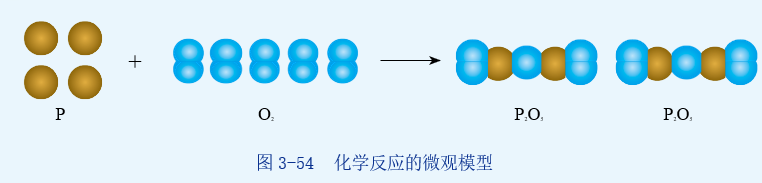
教师点拨:
化学反应的过程就是反应物分子里的原子重新组合成生成物分子的过 程。反应前后原子的种类和数目既没有改变也没有增减,所以,原子的质量没有变化,化学反应前后各物质的质量总和必然相等。
记忆口诀:反应前后:原子数目不变;原子种类不变;原子质量不变。
教师点拨:

质量守恒定律的应用
1.解释一些实验现象
木头燃烧后只剩下灰烬,质量减少了。蜡烛燃烧后留下的蜡油很少,质量减少了?
2.推测一些物质的组成
蜡烛在空气中燃烧生成二氧化碳和水,能否根据这一事实,推断出蜡烛中肯定会有什么元素?可能会有什么元素?
3.进行有关的计算
计算反应物的质量与生成物的质量
氯酸钾24.5克与5克二氧化锰混合后共热,完全反应后,冷却称得剩余固体物质为19.9克,求生成的氧气多少克?
4.化学方程式书写的依据
配平化学方程式
| 学生思考后回答。
学生参与活动,观察后思考,探究反应前后物质总量的变化。
学生参与活动,观察后思考,探究反应前后物质总量的变化。
学生观察后思考,用分子原子的知识加以分析。
学生记录笔记,记忆口诀。
|
课
堂
练
习
| 1.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
物质
| 甲
| 乙
| 丙
| 丁
| 反应前的质量/g
| 30
| 55
| 20
| 70
| 反应后的质量/g
| 0
| 100
| X
| 5
|
根据质量守恒定律判断,X的值为( )
A.50 B.70 C.40 D.15
【答案】B
【解析】根据质量守恒定律,反应前各物质的质量总和等于反应后生成各物质的质量总和,则<Object: word/embeddings/oleObject1.bin>,X=70;故选B。
2.一定质量的铁丝在氧气中完全燃烧后生成四氧化三铁,其固体质量随时间的变化可用下图表示,则用(M2-M1)表示的质量是( )
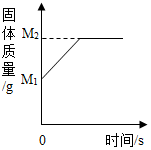
A.参加反应的O2的质量
B.参加反应的Fe的质量
C.生成Fe3O4的质量
D.剩余的O2的质量
【答案】A
【解析】从图示看出,M1表示反应前固体的质量,就是铁丝的质量,M2表示反应后固体的质量,是四氧化三铁的质量,则M2-M1就表示参加反应的氧气的质量。
故选:A。
3.氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示,下列说法不正确的是( )
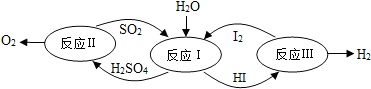
A.该流程可实现太阳能向化学能的转化
B.制得H2中氢元素最初来源于水和硫酸
C.所有涉及的反应中,有四种元素的化合价发生了改变
D.反应I中,发生反应的化学方程式为SO2+I2+2H2O=2HI+H2SO4
【答案】B
【解析】A.根据“以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法”,可知该流程可实现太阳能向化学能的转化,故A正确。
B.反应I的化学方程式为: SO2+2H2O+I2=H2SO4+2HI,根据质量守恒定律可知,制得H2中氢元素最初来源于水,故B错误。
C.反应I中,I的化合价由0转化为-1,S的化合价由+4转化为+6;反应Ⅱ中,O的化合价由-2转化为0,S的化合价由+6转化为+4;反应Ⅲ,H和I由化合态变为游离态,元素的化合价发生了改变,故C正确。
D.由图可知,反应Ⅰ为二氧化硫与碘发生氧化还原反应生成硫酸和HI,化学方程式为: SO2+I2+2H2O=2HI+H2SO4,故D正确。故选B。
|
课
堂
小
结
| 化学方程式是化学领域中一种重要的表达方式,它用化学式精确地描述了化学反应的过程。在书写化学方程式时,我们必须以实验事实为依据,确保方程式的正确性,并且需要符合质量守恒定律,即反应前后元素的原子个数必须保持相等。书写化学方程式的步骤包括写出正确的反应物和生成物化学式,通过配平确保方程式的平衡性,并注明反应条件和生成物的状态。化学方程式不仅代表了化学反应的过程,还承载着丰富的化学意义。在实际应用中,我们可以根据化学方程式进行计算,通过设定未知数、书写方程式、找出相关物质的相对分子质量和已知条件,列出比例式并求解,最后对结果进行简明的回答。这一计算过程为我们理解和量化化学反应提供了有力的工具。
|
板
书
设
计
| 一、质量守恒定律
1.定律内容:
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
2.质量守恒微观解释:
反应前后原子的种类和数目并没有改变,所以化学反应前后各物质的质量总和必然相等。
3.质量守恒定律的应用
|
作
业
设
计
| |
反
思
评
价
| |
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图