教学过程
|
教师活动
| 学生活动
|
新
课
导
入
| 复习引入:
1.氧气的物理性质:①氧气是一种无色无味的气体②不易溶于水③密度比空气大④低温下可液化成蓝色液体,也可凝固成雪花状蓝色固体
2.氧气的化学性质
氧气是一种化学性质比较活泼的气体。
氧气支持燃烧。
3.化合反应
由两种或两种以上的物质生成一种物质的反应叫做化合反应。
| 学生思考,回忆。
|
新知讲授
| 一、思考:生产生活中需要大量的氧气,我们可以通过什么方法获取?
回答:1.空气冷冻分离法
2.膜分离技术
教师补充:空气冷冻分离法利用的原理是沸点不同。
思考:上述两种工业制氧过程,是属于什么变化过程?
回答:都是属于物理变化过程
二、氧气的实验室制法
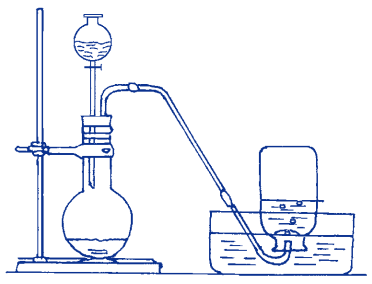
补充:二氧化锰 (MnO2)只起改变反应速度的作用,本身的质量和化学性质在反应前后都没有改变。这种物质叫做催化剂。
教师点拨:催化剂的理解:(1)催化剂能改变化学反应速率,既能加快,也能减慢。(2)催化剂反应前后化学性质不变,但物理性质可能改变。(3)催化剂离不开特定的化学反应。(4)催化剂不能决定反应能否进行。(5)催化剂不能增多或减少生成物的质量。(6)对于同一化学化学反应,可以有多种催化剂;对于不同化学反应,可以使用相同的催化剂。
2.气体的收集方法
根据氧气的物理性质得出向上排空气法(瓶口向上),排水法。
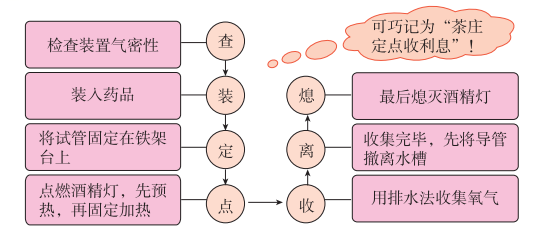
教师点拨:实验室制取气体的装置的选择:(1)根据反应物的状态和反应条件选择发生装置;(2)根据气体的密度和水溶性选择收集装置。气体收集装置的选择原则:“溶不排水,毒不排空,重向上排,轻向下排”。
3.检查装置的气密性
手捂(加热)法
将导管的出口浸入水中,手握试管等容器,如果有气泡从导管口逸出,放手后导管末端回流一段水柱,表明装置不漏气。
4.氧气的工业制法
(1)空气冷冻分离法:利用液氧和液氮的 沸点 不同,通过分离液态空气获得氧气。

(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,可以得到含氧量较高的富集氧气。
三、化合反应和分解反应
在研究氧气的化学性质及制取氧气的过程中,我们接触了许多化学反 应,你是否注意过这些化学反应有什么不同呢?
教师点拨:
1.判断某变化是化合反应还是分解反应,首先判断该变化是否是化学变化,再从形式特征上去判断。
| 学生思考后回答。
学生仔细观察实验,思考后回答。
学生参与活动,观察后思考。
学生参与活动,观察后思考。
|
课
堂
练
习
| 1.如图所示,①为制取氧气的发生装置(气密性良好),其中的燃烧匙可以上下移动。②和③为氧气的收集装置。小金欲制取一瓶干燥的氧气,下列分析正确的是( )
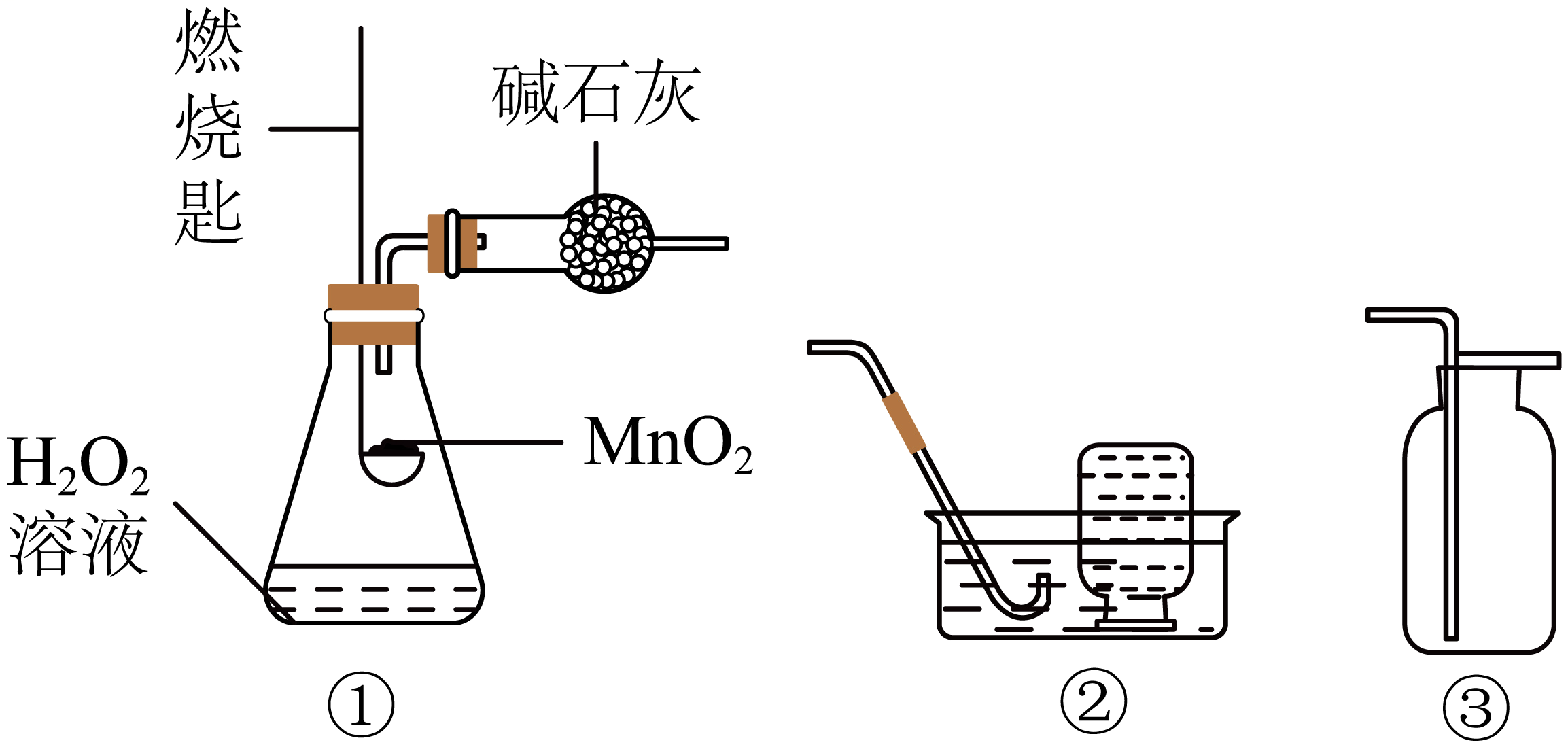
A.在①中,将MnO2浸入H2O2溶液,MnO2可分解产生氧气
B.若用装置②的方法收集氧气,需等到导管口气泡均匀并连续冒出时才可收集
C.若用装置③的方法收集氧气,可将带火星的木条伸入瓶内进行验满
D.将装置①分别与装置②或③连接,均能达到实验目的
【答案】B
【解析】A、在①中,将MnO2浸入H2O2溶液,MnO2可分解产生氧气错误,因为二氧化锰是催化剂,故选项错误;
B、若用装置②的方法收集氧气,需等到导管口气泡均匀并连续冒出时才可收集,故选项正确;
C、若用装置③的方法收集氧气,可将带火星的木条放在集气瓶口验满,故选项错误;
D、将装置①分别与装置②或③连接,均能达到实验目的错误,因为排水法收集的氧气不干燥,故选项错误;
故选B。
2.小马同学将一定量的氯酸钾与少量高锰酸钾的混合物加热制取氧气,部分物质质量随时间的变化如图所示,下列有关叙述正确的是( )
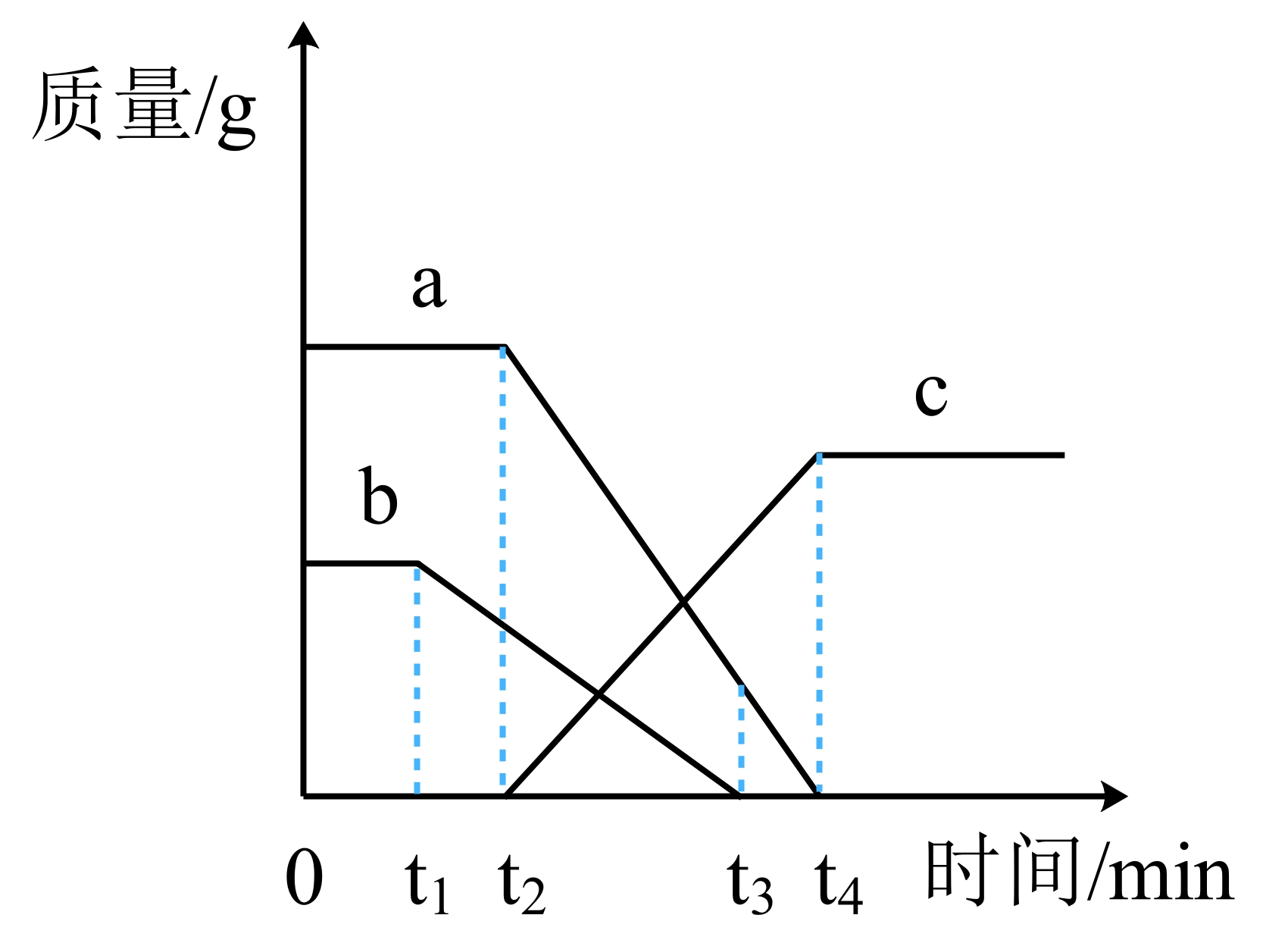
A.在t1至t2时间内,氯酸钾的质量在减少
B.在t3至t4时间内,二氧化锰的质量增加
C.t3时,试管中有4种固体物质
D.曲线c代表加热过程中生成氧气质量的变化
【答案】C
【分析】高锰酸钾加热生成锰酸钾、二氧化锰、氧气,氯酸钾在二氧化锰的催化作用下加热分解生成氯化钾和氧气;
【解析】A、高锰酸钾比氯酸钾更容易反应,故在 t1 至 t2 时间内,高锰酸钾的质量在减少,氯酸钾从t2开始反应,错误;
B、综上分析,b表示高锰酸钾分解,a表示氯酸钾分解,到t4时,高锰酸钾完全反应,则二氧化锰的质量不再增加,在 t3 至 t4 时间内,二氧化锰催化氯酸钾分解,二氧化锰的质量不变,错误;
C、t3 时,试管中有锰酸钾、二氧化锰、氯化钾、氯酸钾4种固体物质,正确;
D、氧气从t1时就开始生成了,曲线c代表加热过程中生成氯化钾质量的变化,错误。
故选C。
3.关于氧气的性质和制取实验,下列说法正确的是( )
A.铁丝在氧气中燃烧,为了实验现象更显著,应该选较粗的铁丝
B.硫在空气中燃烧,发出明亮的蓝紫色火焰
C.加热高锰酸钾制取氧气,实验结束时应先将导管从水中取出,再熄灭酒精灯
D.分解过氧化氢制取氧气,加入二氧化锰目的是为了提高氧气的产量
【答案】C
【解析】A、铁丝在氧气中燃烧,为了实验现象更显著,应该选较细的铁丝,较细的铁丝与氧气的接触面积较大,错误;
B、硫在空气中燃烧,发出微弱的淡蓝色火焰,在氧气中燃烧发出明亮的蓝紫色火焰,错误;
C、加热高锰酸钾制取氧气,实验结束时应先将导管从水中取出,再熄灭酒精灯,以防冷水倒吸,炸裂试管,正确;
D、分解过氧化氢制取氧气,加入二氧化锰目的是为了加快过氧化氢的分解速率,而不是提高氧气的产量,错误。
故选C。
|
课
堂
小
结
| 在今天的课堂上,我们深入探讨了氧气的制备方法,包括工业制法和实验室制法,同时也复习了分解反应的基本概念。
首先,我们了解了氧气的工业制法。其中,空气冷冻分离法是一个重要方法。这种方法基于空气中不同组分在低温下液化温度不同的原理,通过压缩、冷却和蒸馏等步骤,将氧气从空气中分离出来。另外,我们还介绍了膜分离技术,这是一种利用特定材料制成的膜对气体分子的选择性透过性,从而实现氧气和氮气等气体分离的技术。
接着,我们转向氧气的实验室制法。在实验室中,我们通常使用分解反应来制备氧气。分解反应是一种由一种物质生成两种或两种以上物质的反应。在制备氧气的实验中,我们常用的物质有过氧化氢、高锰酸钾等。这些物质在催化剂的作用下,通过分解反应产生氧气。
在实验室制备氧气的过程中,我们需要选择合适的制取装置。这些装置通常包括反应容器、加热装置、气体收集装置等。我们需要根据反应的特点和条件来选择合适的装置,并确保实验过程的安全和准确性。
最后,我们回顾了分解反应的概念。分解反应是一种基本的化学反应类型,它在我们日常生活中和工业生产中都有着广泛的应用。通过今天的学习,我们不仅对氧气的制备方法有了更深入的了解,也对分解反应有了更清晰的认识。
总的来说,今天的课堂内容充实而有趣。我们通过学习氧气的制备方法和分解反应的概念,不仅拓宽了知识面,也提高了实验技能和思维能力。希望同学们能够将这些知识应用到实际生活中去,为未来的学习和工作打下坚实的基础。
|
板
书
设
计
| 氧气的工业制法
1.空气冷冻分离法
2.膜分离技术
氧气的实验室制法
1.制取原理
2.制取装置
由一种物质生成两种或两种以上的物质的反应叫做分解反应
|
作
业
设
计
| |
反
思
评
价
| |
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图