教学过程
|
教师活动
| 学生活动
|
新
课
导
入
| 温故知新,导入新课:
(1)常见的化合物中氢总是+1价,氧总是-2价。金属元素常显正价。
(2)非金属元素跟氧化合时常显正价,跟氢化合时常显负价。
(3)单质中元素的化合价为零价。
(4)在化合物里,元素正负化合价的代数和为零,有些元素在不同的化合物里常显“相同”的化合价,有些元素在不同的化合物里常显“相同”的化合价。

| 学生思考,温故知新,自主探究,完成下列填空。
|
新知讲授
| 一、相对原子质量
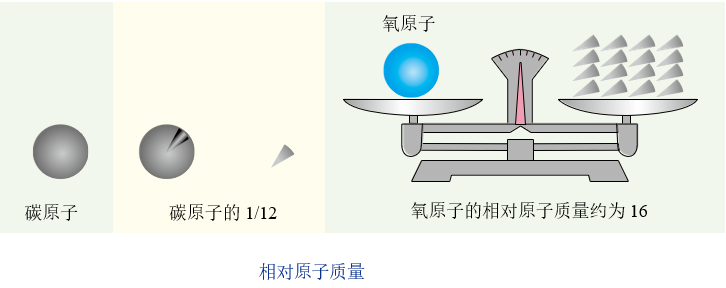
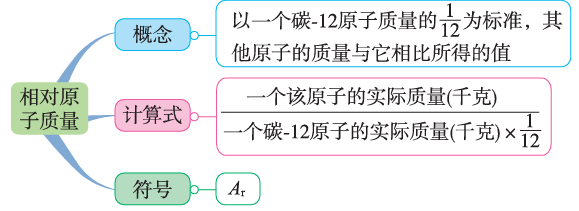
【比较】原子的质量与相对原子质量的比较

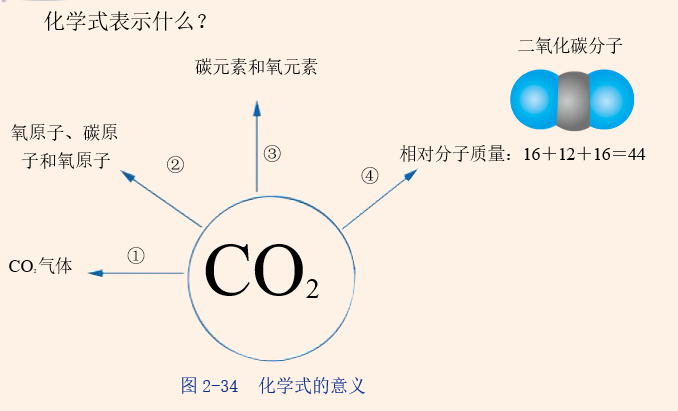
二、相对分子质量
1.相对分子质量的概念和符号
(1)概念:一个分子中各原子的相对原子质量总和就是该分子的相对分子质量。
2.有关相对分子质量的计算
(1)计算方法及公式

(2)注意事项
①元素符号与数字之间在计算相对分子质量时需用“×”;元素符号之间在计算相对分子质量时需用“+”。如C02的相对分子质量的计算方法为12+16×2=44。
②原子团括号外右下角的数字表示其个数,应先将原子团内各原子的相对原子质量之和计算出来,再乘以其个数。如(NH4)2SO4的相对分子质量计算方法为(14+1×4)×2+32+16×4=132。
③结晶水合物中的“·”表示结合的含义,在计算相对分子质量时应将“·”前后两部分各原子的相对原子质量相加而不是相乘。如CuSO4·5H2O的相对分子质量计算方法为64+32+16×4+(1×2+16)×5=250。
三、元素质量分数和质量比的确定
1.计算物质组成元素的质量比

2. 计算物质中某元素的质量分数
(1)含义:物质中某元素的质量分数,就是该元素的质量与组成物质的元素总质量之比。

3.氮肥
氮肥是含有氮元素的物质,如碳酸氢铵(NH4HCO3)、尿素[CO(NH2)2]、硫酸铵[(NH4)2SO4]、硝酸铵(NH4NO3)。各种氮肥中的氮元素的质量分数不相同。
| 学生思考,积极参与课堂。
学生思考,积极参与课堂。
学生思考,积极参与课堂。
学生思考,积极参与课堂。
|
课
堂
练
习
| 1.在FeSO4和Fe2(SO4)3的混合物中,氧元素的量分数为a%,则铁元素的质量分数为( )
A.1-a% B.1-3a% C.1-1.5a% D.1.5a%
【答案】C
【解析】在FeSO4和Fe2(SO4)3组成的混合物中,硫元素与氧元素的质量比=32:(16×4)=1:2,由于混合物中氧元素的质量分数为a%,则混合物中硫元素质量分数为0.5a%,铁元素的质量分数是:1-a%-0.5a%=1-1.5a%。故选C。
2.将一定量xFeSO4•y(NH4)2SO4•6H2O晶体加入过量NaOH溶液中,加热生成NH30.85g(假如生成NH3的全部逸出),过滤、洗涤、灼烧,得Fe2O3固体2.0g.则x,y的关系正确的是( )
A.x:y=1:1 B.x:y=1:2 C.x:y=1:4 D.x:y=2:1
【答案】A
【解析】试题分析:据质量守恒定律可以知道,晶体中的氮元素和氨气中的氮元素的质量相等,而晶体中的铁元素的质量和生成的氧化铁中的铁元素的质量相等,即:
56x:(14×2)y=(2.0g××100%):(0.85g××100%)
解得:x:y=1:1
故选A。
3.已知某元素的原子与碳12原子的质量比为9,则该元素的相对原子质量为( )
A.108 B.1.33 C.108克 D.1.33克
【答案】A
【解析】原子的质量与原子的相对原子质量呈正比,某元素的原子与碳-12原子的质量比为9;碳-12原子的相对原子质量为12,则该元素的原子的相对原子质量为12×9=108。
故选A。
|
课
堂
小
结
| 1.把一个碳-12原子的质量分为12等份,其他原子的质量与一个碳-12原子的质量1/12相比,得出一定的比值,这个比值就是该原子的相对原子质量。
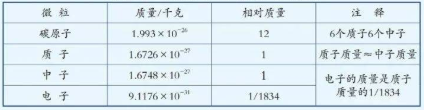
2.查出1~18号元素的相对原子质量,并填在表中。
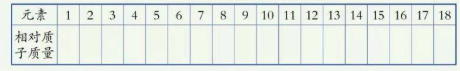
3.相对分子质量:一个分子中各原子的相对原子质量总和就是该分子的相对分子质量。
4.根据化学式,我们可以计算出组成物质的各种元素的质量比。根据化学式,还可以计算物质中某一元素的质量分数。
|
板
书
设
计
| 1.把一个碳-12原子的质量分为12等份,其他原子的质量与一个碳-12原子的质量1/12相比。得出一定的比值,这个比值就是该原子的相对原子质量。
2.相对分子质量:
一个分子中各原子的相对原子质量总和就是该分子的相对分子质量。
|
作
业
设
计
| |
反
思
评
价
| |
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图