教学过程
|
教师活动
| 学生活动
|
新
课
导
入
| 许多物质都能溶解在溶剂里形成溶液,溶液在日常生活和生产中应用广泛。许多化学反应也都要在溶液中才能进行。那么,各种物质在溶解过程中有哪些特性呢?不同物质溶解过程有什么不同呢?

| 观察图片,了解溶解现象。
|
新 知 讲 授
| 一、物质的溶解性
我们已经知道蔗糖能溶解在水中。你是否想过,在一定量的水中不断加入蔗糖,蔗糖能否全部溶解?
活动
1.如图所示,将1药匙蔗糖放入盛有20毫升水的烧杯中,进行充分搅拌,你观察到的现象是 蔗糖逐渐全部溶解 ;
2.逐渐增加放入水中的蔗糖的数量,你观察到的现象是 蔗糖溶解一部分之后不再继续溶解,烧杯底部有固体蔗糖剩余 。

从以上的实验可以发现,一定量的蔗糖能溶解在一定量的水中。当放入水中的蔗糖超过一定量后,无论怎么搅拌或摇晃,一部分蔗糖总是不能溶解。这说明在一定条件下,物质能够溶解的数量是有限的。
溶解性:一种物质(溶质)溶解在另一种物质(溶剂)里的能力。
溶解性是物质的一种物理性质。一般情况下,在一定温度下,在一定量的溶剂里溶质溶解的量是有限的。
二、影响物质溶解性的因素
我们知道,溶液是由溶质和溶剂组成的,不同的溶质在同一种溶剂里的溶解性不同。例如,高锰酸钾易溶于水,而泥沙就难溶于水。还有哪些因素会影响物质的溶解性呢?我们一起来探究。
探究物质溶解性的影响因素
【提出问题】物质的溶解性与哪些因素有关?
【猜想与假设】①不同物质在同种溶剂中溶解能力不同;
②同种物质在不同溶剂中溶解能力不同;
③相同条件下,物质的溶解性与温度有关。
【实验药品】固体药品选用硫酸铜白色粉末、氢氧化钙粉末,溶剂选用水、酒精。
实验1:室温下,在2只烧杯中都装有20毫升的水,分别加入10克的硫酸铜和硝酸钾,并进行搅拌,观察两种物质的溶解情况。
【实验现象】硫酸铜在水中 完全溶解 ;
氢氧化钙在水中 未完全溶解 ;
【实验结论】 不同物质在同种溶剂中的溶解能力不同 。

实验2:在室温下,在2只烧杯中分别装有20毫升的水和20毫升的酒精,分别加入10克的硫酸铜,并进行搅拌,观察硫酸铜的溶解情况。
【实验现象】硫酸铜在水中 完全溶解 ;
硫酸铜在酒精中 几乎没有溶解 ;
【实验结论】 同种物质在不同溶剂中的溶解能力不同 。
实验3:将上述不能完全溶解的硝酸钾用酒精灯加热,并用玻璃棒不断搅拌,观察现象。
【实验现象】 硝酸钾全部溶解了。
【实验结论】 相同条件下,物质的溶解性与温度有关。
从以上实验可以知道:要比较不同物质的溶解性,必须在相同的温度、相同的溶剂并且质量也相等的情况下,该溶质不能再继续溶解时进行比较。以上实验也可以测量物质溶解的质量,用数据进行比较。如下表。
温度既能影响物质的溶解性又能影响物质的溶解速率,而振荡、搅拌、增加溶剂的量、将固体物质研碎只影响物质的溶解速率,不影响物质的溶解性。
| 实验1
| 实验2
| 实验3
| 目的
| 探究同种物质在不同溶剂中的溶解性
| 探究不同物质在同种溶剂中的溶解性
| 探究物质的溶解性是否与温度有关
| 条件控制
| 在相同温度下测量同种溶质在不同种溶剂中溶解的质量
| 在相同温度下测量不同溶质在同种溶剂中溶解的质量
| 在不同温度下测量同种溶质在相同溶剂中溶解的质量
| 实验方案
| 温度控制在20℃,取硫酸铜分别溶解在100克水和100克酒精中,直到不再溶解,分别测量溶解的硫酸铜的质量
| 温度控制在20℃,取硫酸铜和硝酸钾分别溶解在100克水中,直到不再溶解,分别测量溶解的硫酸铜和硝酸钾的质量
| 在烧杯中加入100克水,测量温度,然后逐渐加入硫酸铜直到不再溶解,测量溶解的硫酸铜的质量;然后升高温度,记下温度,再继续加入硫酸铜直至不再溶解,测量溶解的硫酸铜的质量
| 实验数据
| 水中溶解的硫酸铜的质量
酒精中溶解的硫酸铜质量
| 溶解的硫酸铜的质量
溶解的硝酸钾的质量
| 20℃时100克水中溶解硫酸铜的质量
70℃时100克水中溶解硫酸铜的质量
| 结论
| 物质的溶解性与溶剂的性质有关
| 物质的溶解性与溶质的性质有关
| 物质的溶解性与温度有关
|
实验结论:影响固体物质溶解性的因素包括溶质、溶剂的性质及温度。
思考与讨论:打开汽水瓶盖时我们会看到有气泡冒出,而且夏天比冬天现象明显。烧水时水中有气泡冒出,夏天正午河水中的鱼儿纷纷冒出水面,这些事例说明了什么?

气体的溶解能力和温度、气压有关。
三、物质溶解时的吸热、放热现象
生活中我们会接触到很多物质的溶解,如食盐的溶解、蔗糖的溶解……,除了溶解性的不同,你是否留意物质溶解过程中的热量变化呢?物质溶解时,是从外界吸收热量,还是向外界释放热量呢?我们可以设计活动探究这种现象。
实验设计思路
分别取100g水于3个烧杯中。测量水的温度并记录t0℃,分别加入等量的氯化钠、氢氧化钠、硝酸铵于3个烧杯中,用玻璃棒充分搅拌溶解,用温度计测量三个烧杯内溶液的温度,并记录t1℃、t2℃、t3℃。与初始温度进行比较。
活动:取3只烧杯,分别装入100mL水。用温度计测出水的温度,读数是25℃。
在其中的1只烧杯中加入氢氧化钠,并使之溶解,再用温度计测量。温度计的读数是25℃。
在第2只烧杯中加入氢氧化钠,并使之溶解,再用温度计测量。温度计的读数是40℃。
在最后1只烧杯中加入硝酸铵,并使之溶解,用温度计测量。温度计的读数是16℃。

实验分析:
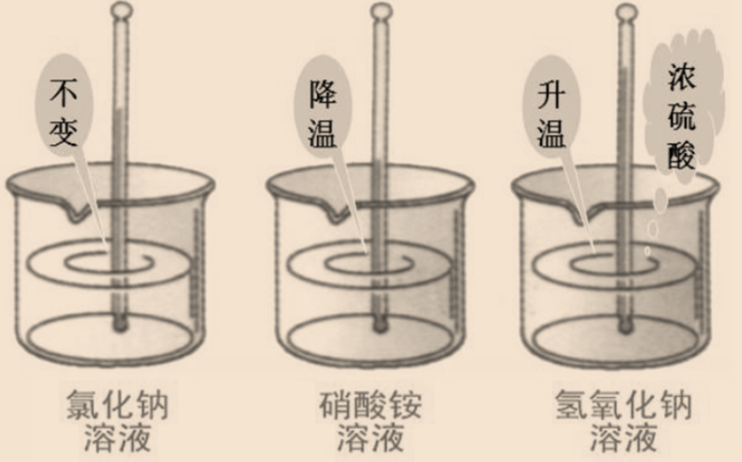
氯化钠溶于水既不吸热也不放热,溶液温度变化不大;氢氧化钠溶于水放热,溶液温度升高;硝酸铵溶于水吸热,溶液温度降低。
实验表明:
有的物质溶解时,会放出热量,使溶液温度升高,如氢氧化钠、浓硫酸等;
有的物质溶解时,会吸收热量,使溶液温度降低,如硝酸铵;
也有许多物质溶解时,溶液的温度没有明显变化,如氯化钠等。
知识拓展
溶解时的吸热或放热现象是指物质在溶解时,所发生的两个过程的吸热和放热的多少不同,而引起的溶液的温度变化的现象。具体来说,物质溶解的过程包含有以下两个过程:
①物质的分子(或离子)向水中扩散,该过程吸收热量;
②物质的分子(或离子)和水分子作用,生成水合分子(或水合离子),该过程放出热量。
1.当溶解时放出的热量>吸收的热量时,表现为放热现象,溶液温度会升高(如氢氧化钠、浓硫酸等);
2.当溶解时放出的热量=吸收的热量时,表现为既不吸热,也不放热的现象。溶液温度不变(如氯化钠等);
3.溶解时放出的热量<吸收的热时,表现为吸热现象,溶液温度会降低(如硝酸铵等)。
| 了解一般情况下,在一定温度下,在一定量的溶剂里溶质溶解的量是有限的。
探究影响物质溶解性的因素,知道控制变量法的应用。
了解影响物质溶解速率的因素。
知道用定量的方法探究物质影响因素的实验方法。
思考影响气体物质溶解性的因素。
了解物质溶解时吸热、放热现象。
|
课
堂
练
习
| 典例1 小金为了探究“影响物质溶解性的因素”,设计如下实验:
实验组别
| A
| B
| C
| D
| 溶液温度
| 20℃
| 20℃
| 60℃
| 20℃
| 溶剂种类
| 水
| 水
| 水
| 水
| 溶剂质量
| 10克
| 10克
| 10克
| 20克
| 溶质种类
| 硝酸钾
| 食盐
| 硝酸钾
| 硝酸钾
| 加入溶质质量
| 10克
| 10克
| 10克
| 10克
| 剩余溶质质量
| 6.9克
| 6.4克
| 0克
| 3.8克
|
(1)该实验通过观察来比较物质的溶解性;
(2)欲探究溶质种类是否影响物质的溶解性,应选A组和组进行比较;
(3)根据A组和C组的结果,可以得到的结论是;
(4)有同学认为,根据A、D两组可以得出,该温度下硝酸钾的溶解性与溶剂质量无关,你认为该说法是否合理?并说明理由。
【答案】(1)剩余溶质质量大小(2)B(3)硝酸钾的溶解性随着温度的升高而增大(4)合理,因为相同温度下,两组实验中所溶解的溶质质量与溶剂的质量之比相等。
【解析】(1)该实验通过观察剩余溶质质量大小来比较物质的溶解性;
(2)A组和B组只有溶质种类不同,其他条件完全相同,可以探究溶质种类是否影响物质的溶解性,故答案为B;
(3)A组与C组只有温度不同,根据A组和C组中剩余固体种类的大小结果,可以得到的结论是硝酸钾的溶解性随着温度的升高而增大,故答案为硝酸钾的溶解性随着温度的升高而增大;
(4)A、D两组只有溶剂的质量不同,A组中,10g水中的溶解硝酸钾的质量为10g-6.9g=3.1g;D组中,20g水中溶解硝酸钾的质量为10g-3.8g=6.2g,所溶解的溶质质量与溶剂的质量之比相等,所以根据A、D两组可以得出,该温度下硝酸钾的溶解性与溶剂质量无关,故答案为:合理,因为相同温度下,两组实验中所溶解的溶质质量与溶剂的质量之比相等。
典例2 海藻酸钠是从褐藻类的海带或马尾藻中提取碘和甘露醇之后的副产物,是一种天然多糖,在食品工业和医药领域得到广泛应用。海藻酸钠在水中的溶解的较慢,使用时需要较长的时间来配制溶液,对日常使用产生了一定的影响。小滨通过查阅资料得知,加入一定量3%浓度的六偏溶液可加快溶解速度。小滨同学按下表进行实验。
实验序号
| 海藻酸钠质量/克
| 水的质量/克
| 水的温度/℃
| 六偏溶液/毫升
| 1
| 1.4
| 100
| 40
| 0
| 2
| 1.4
| 100
| | 2
| 3
| 1.4
| 100
| 40
| 4
| 4
| 1.4
| 100
| 40
| 6
|
(1)按照小滨的实验设计表第2组中水的温度的数据是;
(2)本实验中小滨的实验目的是:探究对海藻酸钠的溶解速度的影响;
(3)为了达成实验目的,小滨应该要通过观察来确定海藻酸钠的溶解快慢(即上述表格中最后一列的表头项目名称)。
【答案】(1)40℃(2)六偏溶液的体积(3)未溶解海藻酸钠的质量的多少
【解析】(1)通过表格中的数据可以看出,在实验中,六偏溶液的体积不同,其他的条件都应该是相同的,因此第2组中水的温度是40℃;
(2)从实验中的数据可以看出,海藻酸钠的质量、水的质量及水的温度都是相同的,只是六偏溶液的体积不同,因此在本实验中,小滨的实验目的是:探究六偏溶液的体积对海藻酸钠的溶解速度的影响;
(3)为了达成实验目的,小滨应该要通过观察未溶解海藻酸钠的质量的多少来确定海藻酸钠的溶解快慢。
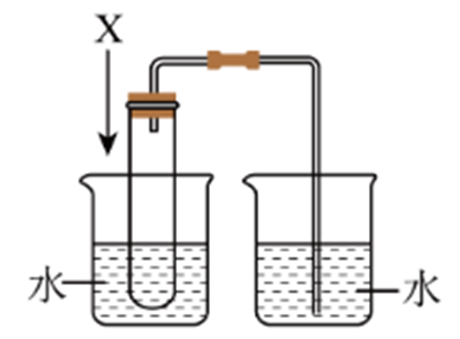
典例3 如图所示,该装置的气密性良好,在左边烧杯中,放入下列哪一种物质后,会在右边导管口形成一段水柱( )
A.氢氧化钠
B.硝酸铵
C.氯化钠
D.氢氧化钙
【答案】B
【解析】在右边导管口形成一段水柱,说明物质溶于水,吸收热量,导致试管内气压减小。
A.氢氧化钠溶于水,溶液温度升高,导致试管内气体受热膨胀,右边导管口会出现气泡,错误;
B.硝酸铵溶于水,溶液温度降低,导致试管内气压减小,右边导管口会形成一段液柱,正确;
C.氯化钠溶于水,溶液温度不变,没有明显现象,错误;
D.氢氧化钙溶于水温度几乎无变化,没有明显现象,错误。
故选B。
典例4 某科学兴趣小组在学习物质溶解的过程后,对氯化铵、氯化钙、氯化钠三种物质溶于水过程中的热量变化进行了探究。
【实验探究】三种物质各取1药匙于烧杯分别溶于水,另外一只烧杯只加水,用温度计测量液体温度,并记录有关数据如下:
实验
| 水的体积
| 所加物质
| 测量液体温度(℃)
| 实验1
| 50mL
| 氯化铵
| 15
| 实验2
| 50mL
| 氯化钙
| 28
| 实验3
| 50mL
| 氯化钠
| 21
| 实验4
| 50mL
| 无
| 22
|
【数据分析】(1)比较实验2与实验4,可获得结论是;
(2)如果要生产一种“冰袋”用于冷敷,上述三种物质中最合适的是;
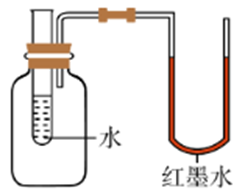
(3)向如图装置的试管中加入上述某种物质后,U形管右边支管的红墨水液面上升,左边支管的红墨水液而降低,则加入的物质是;
【反思评价】(4)经讨论认为本实验操作中存在缺陷,它是。
A.四只烧杯中加入水的体积相同
B.加入物质的质量可能不相等
C.加入物质的种类不一样
【答案】(1)氯化钙溶解过程中放热(2)氯化铵(3)氯化钙(4)B
【解析】(1)比较实验2与实验4,往水中加入氧化钙后,温度升高,因此可获得结论是氯化钙溶解过程中放热;
(2)如果要生产一种“冰袋”用于冷敷,说明这种物质溶解时吸热,从表中可以看出上述三种物质中氯化铵溶解时吸热;
(3)向如图装置的试管中加入上述某种物质后,U形管右边支管的红黑水液面上升,左边支管的红墨水液而降低,则加入的物质溶于水时放出热量,则该物质是氯化钙;
(4)A.实验操作过程中加入等量的水,否则会影响实验效果,故A不符合题意;
B.加入物质的质量必须相等,否则影响实验效果,故B符合题意;
C.探究的就是氯化铵、氯化钙、氯化钠三种物质溶于水过程中的热量变化,因此加入物质的种类不会影响实验,故C不符合题意;
故选B。
|
课
堂
小
结
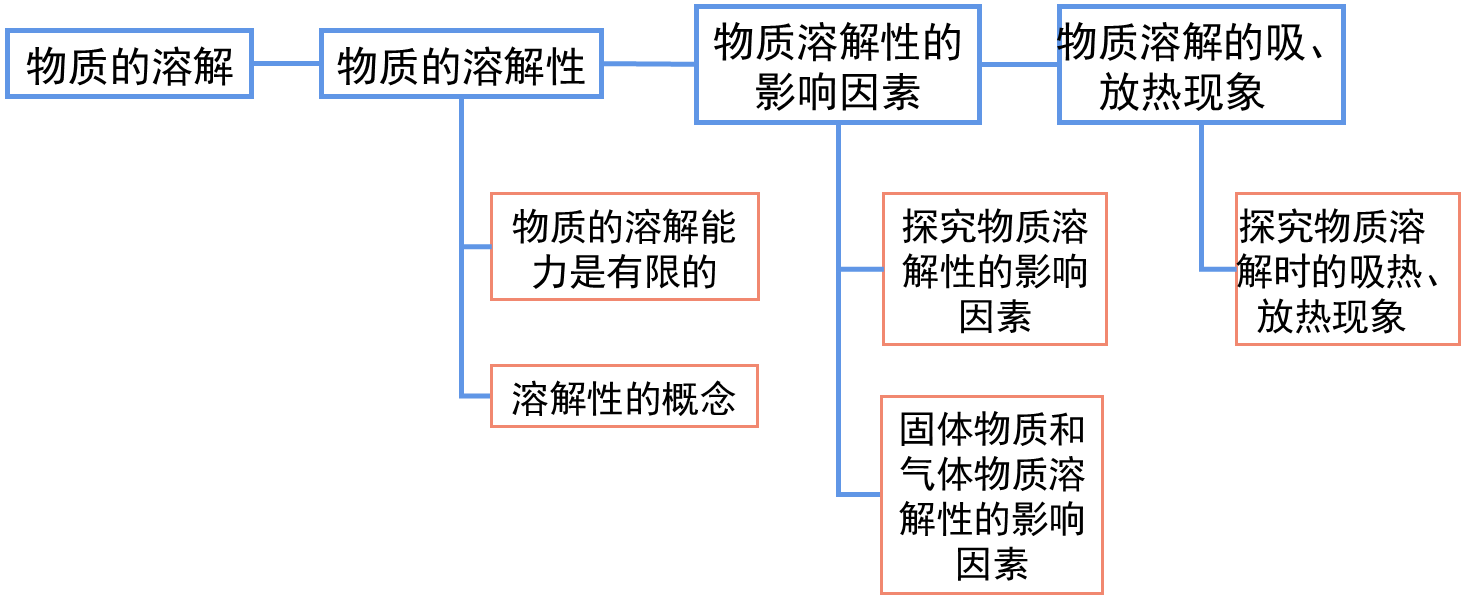
| 1.物质的溶解性
在一定条件下(一定温度下,一定量的溶剂中)物质能够溶解的数量是有限的。
溶解性:一种物质(溶质)溶解在另一种物质(溶剂)里的能力。
2.物质溶解性的影响因素
外因:温度、压强(气体)
内因:溶质性质、溶剂性质
探究方法:控制变量法
3.物质溶解时吸热、放热现象
有的物质溶解时,会放出热量,使溶液温度升高,如氢氧化钠;
有的物质溶解时,会吸收热量,使溶液温度降低,如硝酸铵;
也有许多物质溶解时,溶液的温度没有明显变化,如氯化钠等。
|
板
书
设
计
|
|
作
业
设
计
| |
反
思
评
价
| |
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图