|
|
人教版九年级化学下册
《实验活动8 常见酸、碱的化学性质》教学设计
【教材分析】
本节课是人教版九年级化学下册第十单元的实验活动8。在此之前学生已经学习了酸和碱的化学性质,初步掌握取用药品、酒精灯使用等实验基础技能,这些知识与技能为本节课的实验活动起到了铺垫的作用。本节课对酸、碱的化学性质的实验探究既巩固了前面所涉及的知识点,锻炼了实验操作技能,又加深了对酸碱化学性质的理解与掌握,从理论到实践的角度认识酸、碱的化学性质。通过实验操作,有助于学生掌握酸、碱的化学性质,掌握基本操作技能,学
会观察、记录与归纳描述并交流分享。提高设计方案解决实际问题的能力。体会学以致用,感受化学与生活的密切联系。
【学情分析】
学生已初步认识了酸、碱的化学性质。知道用酸能与指示剂作用,能与活泼金属、金属氧化物、碱溶液反应;知道碱能与指示剂作用,能与酸、盐溶液反应。但该认识还较表面,停留在课本理论知识上,缺乏实验操作与生活现象的支撑。在基本实验知识和操作技能方面,学生初步具备并能够在教师指导下完成实验,得到较直观的结论,但是观察记录与描述表达实验现象、收集证据与分析实验结论、独立设计实验并解决实际问题的能力尚显薄弱。通过创设特定的教学情境,引导学生动手实验与思考交流,能激发学生的学习和探究兴趣,灵活掌握和应用知识。。
【教学目标】
1.通过化学实验及相关分析,进一步理解酸、碱的各项化学性质。
2.通过实验探究,提高实验分析能力和设计实验的能力,进一步了解酸、碱的各项化学性质,酸碱的中和反应。
3.通过探究,能体验到探究活动的乐趣和学习成功的喜悦,并进而增加学习化学的兴趣,通过学生分组实验使学生认识到实验是学习化学的重要途径,并培养同学之间的合作能力。
【教学重点】
巩固几种常见酸碱的物理性质、特性,巩固酸碱的重要化学性质。
【教学难点】
能运用酸碱的知识解决一些实际问题。
【教学方法】
实验学习法、探究学习法、合作学习法、引导探究、讲练结合
【教学准备】
教师准备:白色点滴板、试管、镊子、蒸发皿、坩埚钳、玻璃棒、药匙、酒精灯、铁架台(带铁圈)、胶头滴管、火柴。
稀盐酸、稀硫酸、氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、pH试纸、生锈的铁钉。
还需要:氯化钠溶液、柠檬酸。
【教学过程】
实验目的:
1.加深对酸和碱的主要性质的认识。
2.通过实验解释生活中的一些现象。
实验用品:
白色点滴板、试管、镊子、蒸发皿、坩埚钳、玻璃棒、药匙、酒精灯、铁架台(带铁圈)、胶头滴管、火柴。
稀盐酸、稀硫酸、氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、pH试纸、生锈的铁钉。
还需要:氯化钠溶液、柠檬酸。
【新课导入】你吃柠檬、Vc时,是否感觉很酸?
你能否用学过的知识,采用可行的方法确定其中含有酸?在前面我们学习酸和碱的各化学性质时,大家都只是看到教师的演示实验,今天,让我们自己动手操作,来探究一下酸和碱的各项化学性质。引入新课。
新知探究:
一、酸和碱与指示剂的作用
检查实验桌上的仪器用品是否齐全?
实验活动一:取点滴板,向其中四个穴分别滴加2-3滴稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液,然后分别滴加2-3滴紫色石蕊溶液。
取点滴板,向其中四个穴分别滴加2-3滴稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液,然后分别滴加2-3滴无色酚酞。
实验结论:
酸性溶液使紫色石蕊溶液变红色,不能使无色酚酞溶液变色,
碱性溶液能使紫色石蕊变蓝,使无色酚酞变红色。
2.选择实验室或生活中的几种溶液,进行下列实验:
(1)分别用石蕊溶液和酚酞溶液检验溶液的酸碱性;
(2)用pH试纸测定溶液的酸碱度。
二、金属和金属氧化物与酸的作用
3.(1)取两个生锈的铁钉分别放入两支试管中,然后各加入约2mL稀盐酸,观察现象。
(2)当观察到铁钉表面没有铁锈,铁钉变得光亮时,将其中一支试管中的铁钉取出,
洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,洗净。
比较两个铁钉。
实验现象:(1)锈钉表面的铁锈逐渐消失变得光亮,溶液变成黄色;
(2)当铁钉变得光亮后,可观察到铁钉表面出现气泡。
长时间反应后的铁钉比提前取出的铁钉小。
实验目的:考察铁及其氧化物的化学性质,特别是它们与稀盐酸的反应。
化学方程式:Fe2O3 + 6HCl=2FeCl3 + 3H2O
Fe + 2HCl=FeCl2+ H2↑
【金属与酸的反应】:
镁和盐酸:Mg + 2HCI = MgCl2 + H2↑
锌和盐酸:Zn + 2HCl = ZnCl2 + H2↑
铁和盐酸:Fe + 2HCI = FeCl2 + H2↑
镁和硫酸:Mg + H2SO4 = MgSO4 + H2↑
锌和硫酸:Zn + H2SO4 = ZnSO4 + H2↑
铁和硫酸:Fe + H2SO4 = FeSO4 + H2↑
实验结论:金属+酸→盐+氢气
【金属氧化物与酸的作用】
实验步骤:取黑色固体氧化铜于试管中,然后分别加入稀盐酸、稀硫酸观察现象。
实验现象:黑色固体溶解,溶液变为蓝色。
CuO + H2SO4 = CuSO4 + H20
CuO + 2HCl = CuCl2 + H2O
Fe2O3 + 3H2SO4= Fe2(SO4)3+ 3H2O
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
实验结论:金属氧化物+酸→盐+水
三、碱与盐和酸的作用
4.在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象。再向试管中加入稀盐酸,观察现象。
【实验现象】:生成蓝色沉淀,溶液变为无色;
蓝色沉淀消失,溶液由无色变为蓝色。
【化学方程式】:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
Cu(OH)2+ 2HCl=CuCl2 + 2H2O
【实验结论】:碱+酸→盐+水
盐 + 碱 → 新 碱 + 新盐
四、碱与酸的作用
5.(1)在试管中加入约1mL氢氧化钠溶液,滴入几滴酚酞溶液。然后边用滴管慢慢滴入稀盐酸,边不断振荡试管,至溶液颜色恰好变成无色为止。
(2)取上述反应后的无色溶液约1mL,置于蒸发皿中加热,使液体蒸干,观察现象。
【实验现象】:
溶液滴加酚酞变为红色;
滴加稀盐酸溶液由红色变成无色。
玻璃片出现白色固体。
【化学方程式】:HCI+ NaOH=NaCl+ H2O
6.(1)向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),然后各加入约1mL水,振荡;再各滴入两滴酚酞溶液,观察现象。
(2)继续向其中一支试管中加入约1mL水,振荡;向另一支试管中加入约1mL稀盐酸,振荡;比较两支试管中的现象。
【实验现象】:
1.试管中出现白色浑浊液体
2.白色浑浊液体变为红色澄清液体,另一试管中仍然是红色浑浊液体。
3.红色浑浊液体变为无色澄清的溶液
【实验结论】:
①氢氧化钙不易溶于水,即微溶于水。
②无色酚酞溶液遇碱溶液显示红色。
因氢氧化钙粉末逐渐被酸溶解形成无色溶液。
【问题与交流】该实验可以验证氢氧化钙的哪些性质?
1.氢氧化钙微溶于水。
2.氢氧化钙溶液显碱性,能使酚酞溶液变红色。
3.氢氧化钙能与稀盐酸反应。
巩固提升:
【提出问题】:将一只生鸡蛋放到盛有盐酸溶液的容器中,将出现的现象是鸡蛋上浮又下沉又上浮……,请解释为什么会出现这种现象。
因为当鸡蛋放入足量稀盐酸的玻璃杯中,受重力作用而下沉,碳酸钙与盐酸发生反应生成了二氧化碳气体附着在蛋壳表面而使蛋壳的浮力逐渐大于重力,而使得蛋壳上浮;当上升到一定时, 附着在蛋壳表面的二氧化碳气泡破裂而使浮力小于重力,所以又会下沉。
【学完本课你知道了什么?】
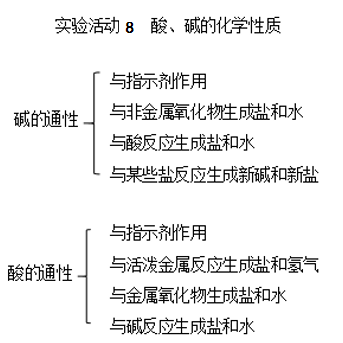
酸的通性:
与指示剂作用;与活泼金属反应生成盐和氢气;与金属氧化物生成盐和水;与碱反应生成盐和水。
碱的通性:
与指示剂作用;与非金属氧化物生成盐和水;与酸反应生成盐和水;与某些盐反应生成新碱和新盐。
【板书设计】
【课后作业】
总结实验中遇到的问题并写出解决方案。
【教学反思】
亮点:本节课重点是通过实验让学生掌握酸、碱的主要化学性质。1.酸、碱能和指示剂反应。2.酸能和金属、金属氧化物和碱反应。3.碱能和酸、盐的反应。学生通过实验探究,以表格的形式进行处理问题,填写表格内容并总结化学性质,体现了学生学习的自主性。学生通过实验解释生活的一些现象。学生在实验时能逐步养成善于观察对比、敢于质疑、参与实验、交流合作的学习方法。通过实验探究增强学生合作学习的意识。
不足:以学生的探究活动为主,在活动中用问题引导学生进行思考,充分发挥学生的主体地位。
- 教学建议:以后的教学,更多的使用小组合作抓住学生,运用探究式的教学方法,充分调动学生的积极性。
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图