教学过程
|
教师活动
| 学生活动
|
新
课
导
入
| 思考引入:
二氧化碳(Carbon dioxide)在空气中含量不多,约占0.03%。然而,就是这些含量很少 CO2,在自然界中却有着不可替代的重要作用。你知道它有哪些重要作用吗?
| 学生思考,自主探究,回答问题。
|
新知讲授
| 一、自然界中的二氧化碳
二氧化碳是由大量二氧化碳分子 (CO2) 聚集而成,每个二氧化碳分子由一个碳原子和两个氧原子构成,其分子结构模型如图所示。
CO2 本身没有毒性,但当空气中的 CO2 超过正常含量时,会对人体产生有害的影响。

二氧化碳对人体健康的影响
空气中 CO2 的体积分数
| 对人体的影响
| 1%
| 感到气闷、头晕、心悸
| 4% ~ 5%
| 感到气闷、头痛、眩晕
| 10% 以上
| 使人神志不清、呼吸停止,以致死亡
|
思考与讨论:为什么冬天虽然天气寒冷,但我们的教室还是应当适时开窗通风?
学生回答:冬天虽然天气寒冷,但我们的教室还是应当适时开窗通风,这是因为室内环境在封闭状态下容易积聚各种有害气体和微生物。人体呼吸会产生二氧化碳,如果长时间不通风,二氧化碳浓度会升高,导致室内空气质量下降,影响人们的呼吸健康。
二、二氧化碳的物理性质研究
活动一: 观察一瓶二氧化碳气体,它的颜色、状态和气味是怎样的?

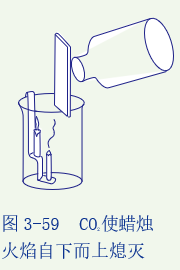
活动二:如图所示,向烧杯里倾倒二氧化碳。注意观察蜡烛火焰的变化现象。
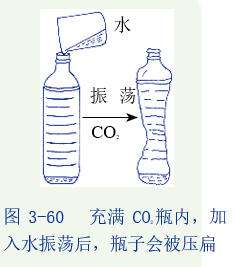
活动三:如图所示,在一个充满二氧化碳的软塑料瓶里,迅速倒入少量蒸馏水,立即将瓶塞塞紧振荡,观察有什么现象。
思考与讨论:同学们能总结出二氧化碳的物理性质吗?
教师点拨:
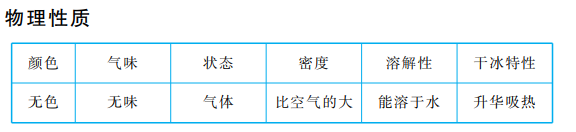
二氧化碳在通常状态下,是一种无色、无味的气体。它的密度比空气的密度大,因此能像倒液体那样从一个容器向另一个容器倾倒。
二氧化碳能溶于水中,通常1体积水中能溶解1体积的CO2,增大压强 可使其溶解得更多。汽水等碳酸饮料就是利用了CO2这一性质制成的。在加压降温的情况下,CO2 能变成无色液体,甚至变成雪状固体,通常人们把固体CO2 叫做“干冰”。
三、二氧化碳的化学性质研究
思考与讨论:CO2溶于水的过程中,有没有发生化学变化呢?
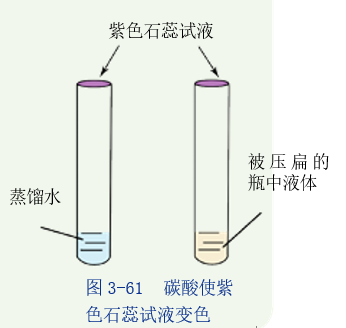
活动一:如图,取2支试管,分别加入少量蒸馏水及图3-54中被压扁的瓶中液体。然后,分别滴加少量紫色石蕊试液,观察2支试管中液体颜色的变化。
活动二:用酒精灯加热颜色呈红色的那支试管,颜色如何变化?
思考与讨论:通过前面的学习,你知道二氧化碳具有哪些化学性质?
教师点拨:

| 学生思考后回答。
学生参与活动,观察后思考,探究二氧化碳物理性质。
学生参与活动,观察后思考,探究二氧化碳物理性质。
学生参与活动,观察后思考,探究二氧化碳物理性质。
学生记录笔记。
学生参与活动,观察后思考,探究二氧化碳化学性质。
学生参与活动,观察后思考,探究二氧化碳化学性质。
|
课
堂
练
习
| 1.化学源于生活,也服务于生活,下列说法不正确的是( )
A.CO和CO2都有毒 B.生铁和钢是含碳量不同的两种铁合金
C.不能用工业盐(NaNO2)烹饪食物 D.合成药物的研发和使用,保障了人体健康
【答案】A
【解析】试题分析:一氧化碳有毒,二氧化碳没有,A错误;铁的合金和生铁和钢,它们的区别是含碳量不同,B正确;亚硝酸钠有毒,C正确。故选A。
2.在实验室中,同学们用如图装置制取纯净的CO2,下列说法不正确的是( )
[查阅资料]饱和碳酸氢钠溶液可以吸收HCl而不吸收CO2;AgNO3溶液遇HCl会产生白色沉淀。
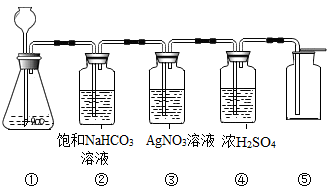
A.①中固体反应物也可用Na2CO3固体代替
B.③中没有白色沉淀产生,说明CO2气体中已经不混有HCl气体
C.④中浓H2SO4的作用是吸收CO2气体中混有的H2O
D.将燃着的小木条放在⑤中的集气瓶口,可以检验集气瓶是否收集满CO2
【答案】A
【解析】A、用碳酸钠代替碳酸钙会使得生成二氧化碳的速率太快不利于气体的收集,所以不能用Na2CO3固体代替,说法错误;
B、氯化氢能和硝酸银溶液反应生成氯化银沉淀,所以③中没有白色沉淀产生,说明CO2气体中已经不混有HCl气体,说法正确;
C、浓硫酸具有吸水性,所以④中浓H2SO4的作用是吸收CO2气体中混有的H2O,说法正确;
D、二氧化碳不燃烧也不支持燃烧,所以可用燃着的小木条放在⑤中的集气瓶口,可以检验集气瓶是否收集满CO2,说法正确。
故选:A。
3.小辉将一大烧杯倒扣在培养皿上,培养皿上所放物质,如图所示。下列对有关实验现象的描述肯定不正确的是( )
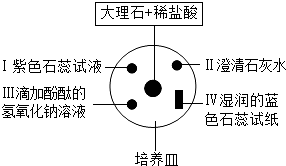
A.Ⅰ处试液变蓝
B.Ⅱ处溶液变浑浊
C.Ⅲ处溶液颜色逐渐变浅
D.Ⅳ处试纸变红
【答案】A
【解析】A、I处是紫色的石蕊试液,二氧化碳溶于水成为碳酸,呈酸性石蕊会变红,符合题意;
B、II处是石灰水,石灰水遇到二氧化碳会变浑浊,不符合题意;
C、III处是氢氧化钠溶液,它会与二氧化碳反应生成碳酸钠,溶液的碱性会减弱,不符合题意;
D、IV处是湿润的蓝色的石蕊试纸,二氧化碳溶于水中时试纸上形成碳酸,使试纸变红,不符合题意。故选A。
|
课
堂
小
结
| 一、自然界中的二氧化碳
二氧化碳(CO₂)是一种无色、无味的气体,是自然界中非常重要的化合物之一。它在地球的大气层中占有一定的比例,是地球气候系统中的重要组成部分。二氧化碳主要由生物呼吸、燃烧过程以及自然过程如火山喷发等产生。
二、二氧化碳的物理性质
1. 密度:在标准条件下,二氧化碳的密度比空气大。
2. 熔点与沸点:在标准大气压下,二氧化碳的熔点为-56.6℃(216.55K),沸点为-78.5℃(194.65K)。
3. 溶解性:二氧化碳在水中的溶解度较高,可以形成碳酸。
4. 三态变化:随着温度和压力的变化,二氧化碳可以在固态、液态和气态之间转化。
三、二氧化碳的化学性质
1. 酸性氧化物:二氧化碳是一种酸性氧化物,可以与水反应生成碳酸。
2. 与碱反应:二氧化碳可以与碱反应生成盐和水。例如,与氢氧化钠反应生成碳酸钠和水。
3. 氧化还原性质:在一定条件下,二氧化碳可以参与氧化还原反应。例如,在高温下,二氧化碳可以被碳还原成一氧化碳。
4. 参与光合作用:在植物的光合作用中,二氧化碳是重要的原料之一。植物通过叶绿体吸收二氧化碳和水,经光合作用生成有机物和氧气。
二氧化碳的这些性质使其在工业、能源、环境等领域具有广泛的应用。例如,二氧化碳可用于生产碳酸饮料、尿素等化学品,还可作为工业制冷剂和灭火剂等。然而,随着人类活动的增加,大气中二氧化碳的浓度不断上升,导致全球气候变暖等环境问题,因此,减少二氧化碳排放、实现低碳发展已成为全球关注的焦点。
|
板
书
设
计
| 一、自然届中的二氧化碳
二、二氧化碳的物理性质
三、二氧化碳的化学性质
|
作
业
设
计
| |
反
思
评
价
| |
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图