教学过程
|
教师活动
| 学生活动
|
新
课
导
入
| 科学家发现每一种化合物都有特定的组成,例如,甲烷分子由碳与氢 原子构成,这两种原子的个数比为1比4,其化学式为CH4。

| 学生思考,自主探究。
|
新知讲授
| 一、化学价
1.化合价的含义
不同元素的原子在形成化合物时,原子之间相互化合的数目。
2.化合价的表示方法

【比较】化合价与离子符号的区别与联系
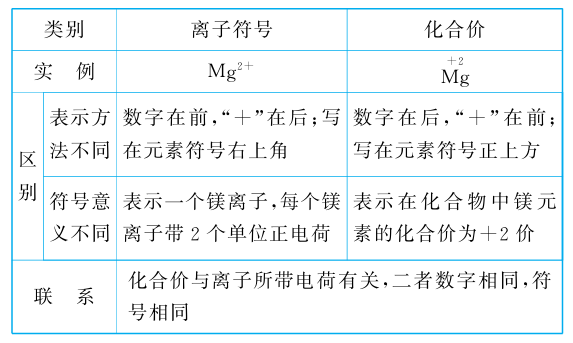
3.化合价规律
(1)金属元素通常显正价,非金属元素通常显负价。
(2)在常见化合物中氧元素通常显一2价,氢元素通常显+1价。
(3)在化合物里,元素正、负化合价的代数和为零。
(4)在单质中,元素的化合价为0。
(5)有些元素在不同的化合物里可能显示相同的化
合价;有些元素在相同的化合物里可能显示不同的化合价。
(6)原子团的化合价一般不为零,其数值由组成元素的正、负化合价代数和决定,与所带电荷相同。
4.化合价的应用
(1)由已知组成元素的化合价推求化合物的化学式。
例:已知磷与氧组成的一种化合物中磷为+5价,氧为-2价,写出该化合物的化学式。
解:最小公倍数法。

答:该化合物的化学式为P2O5。
(2)根据化学式,确定某元素的化合价。
①依据:化合物中,所有元素的正、负化合价代数和为零。
②方法:设待求元素化合价为x,列代数式求解。
例:试求KMnO4中Mn元素的化合价。
解:已知化合物中K元素为+1价,O元素通常为-2价。设Mn元素化合价为x,则依据化合物中元素正、负化合价代数和为零,有:(+1)+x+(一2)×4=0,x=+7。答:KMnO4中Mn元素的化合价为+7价。
教师点拨:书写化学式时,一般按正价元素在前,负价元素在后的顺序写。但有些比较特殊,负价元素在前,正价元素在后,如NH3、CH4等。
教师点拨:单质中只有一种元素,没有化合,故单质中元素化合价为0价。

| 学生思考,积极参与课堂。
学生思考,积极参与课堂。
学生思考,积极参与课堂,积极记笔记。
|
课
堂
练
习
| 1.分子和原子的主要区别是( )
A.分子是构成物质的微粒,原子不是构成物质的微粒
B.分子由原子构成,所以分子的质量都大于原子质量
C.分子在不停地运动,原子在分子中不可能运动
D.分子在化学反应中可分,原子在化学反应中不可再分
【答案】D
【解析】A、构成物质的三种微粒:分子、原子、离子,故A错;
B、分子和原子不能笼统的比较大小,有的分子质量大于有的原子质量,有的原子质量大于有的分子质量,故B错;
C、分子和原子都在不断运动,故C错;
D、在化学反应中分子可以再分,原子不能再分,原子是化学变化中的最小粒子,故D正确。
故选D。
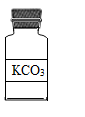
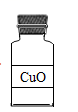
2.试剂瓶的标签上化学式书写错误的是
A.
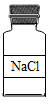 B.
B.
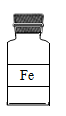 C.
C.
 D.
D.
【答案】C
【解析】A、氯化钠中钠元素显+1价,氯元素显-1价,其化学式为:NaCl,故选项化学式书写正确。
B、铁属于金属单质,直接用元素符号表示其化学式,其化学式为Fe,故选项化学式书写正确。
C、碳酸钾中钾元素显+1价,碳酸根显-2价,其化学式为K2CO3,故选项化学式书写错误。
D、氧化铜中铜元素显+2价,氧元素显-2价,其化学式为:CuO,故选项化学式书写正确。
故选C。
|
课
堂
小
结
| 1.原子之间相互化合的数目,用“化合价”来表示。氢(H)的 化合价为+1,氧(0)为-2,且在化合物中所有元素化合价的代数和为零。 氢或氧与其他元素组成化合物时,根据化合价的代数和为零的原则即可推出各元素的化合价。
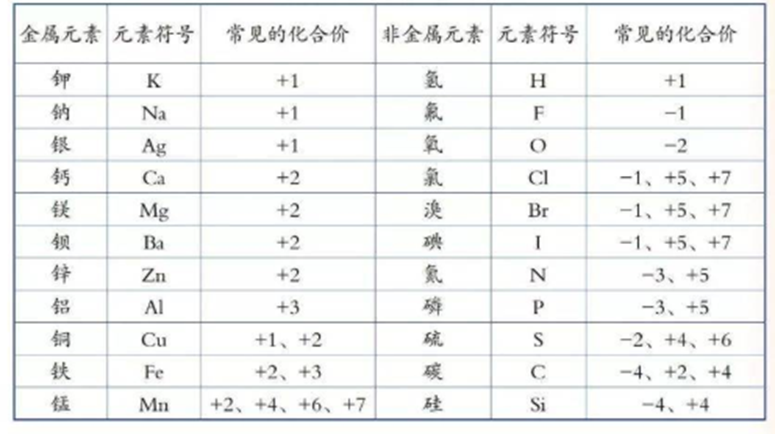
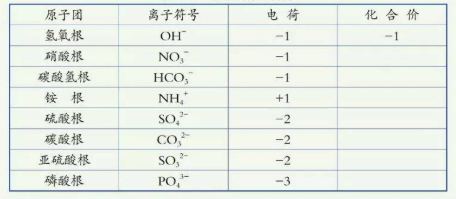
2.原子团中各元素化合价的代数和就是该原子团的化合价。根据元素化合价,
可正确写出化合物的化学式。
(1)常见的化合物中氢总是+1价,氧总是-2价。金属元素常显正价。
(2)非金属元素跟氧化合时常显正价,跟氢化合时常显负价。
(3)单质中元素的化合价为零价。
(4)在化合物里,元素正负化合价的代数和为零,有些元素在不同的化合物里常显“相同”的化合价,有些元素在不同的化合物里常显“相同”的化合价。
|
板
书
设
计
| 1.原子之间相互化合的数目,用“化合价”来表示。
2.原子团中各元素化合价的代数和就是该原子团的化合价。根据元素化合价,
可正确写出化合物的化学式。
(1)常见的化合物中氢总是+1价,氧总是-2价。金属元素常显正价。
(2)非金属元素跟氧化合时常显正价,跟氢化合时常显负价。
(3)单质中元素的化合价为零价。
(4)在化合物里,元素正负化合价的代数和为零,有些元素在不同的化合物里常显“相同”的化合价,有些元素在不同的化合物里常显“相同”的化合价。
|
作
业
设
计
| |
反
思
评
价
| |
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图